Parámetros Séricos en la Evaluación del Estado Nutricional
INTRODUCCIÓN
La valoración nutricional en pacientes con enfermedad renal crónica (ERC) debe ser integral y considerar múltiples parámetros bioquímicos, ya que ningún marcador aislado es suficiente para diagnosticar el estado nutricional.
A pesar de ser una pieza clave debe interpretarse con cautela en la ERC, porque muchos marcadores se modifican por inflamación, sobrehidratación, pérdidas proteicas, comorbilidad y el propio grado de insuficiencia renal. Por ello, su utilidad es mayor cuando se analizan en tendencia, integrados con la clínica, la ingesta y la composición corporal.
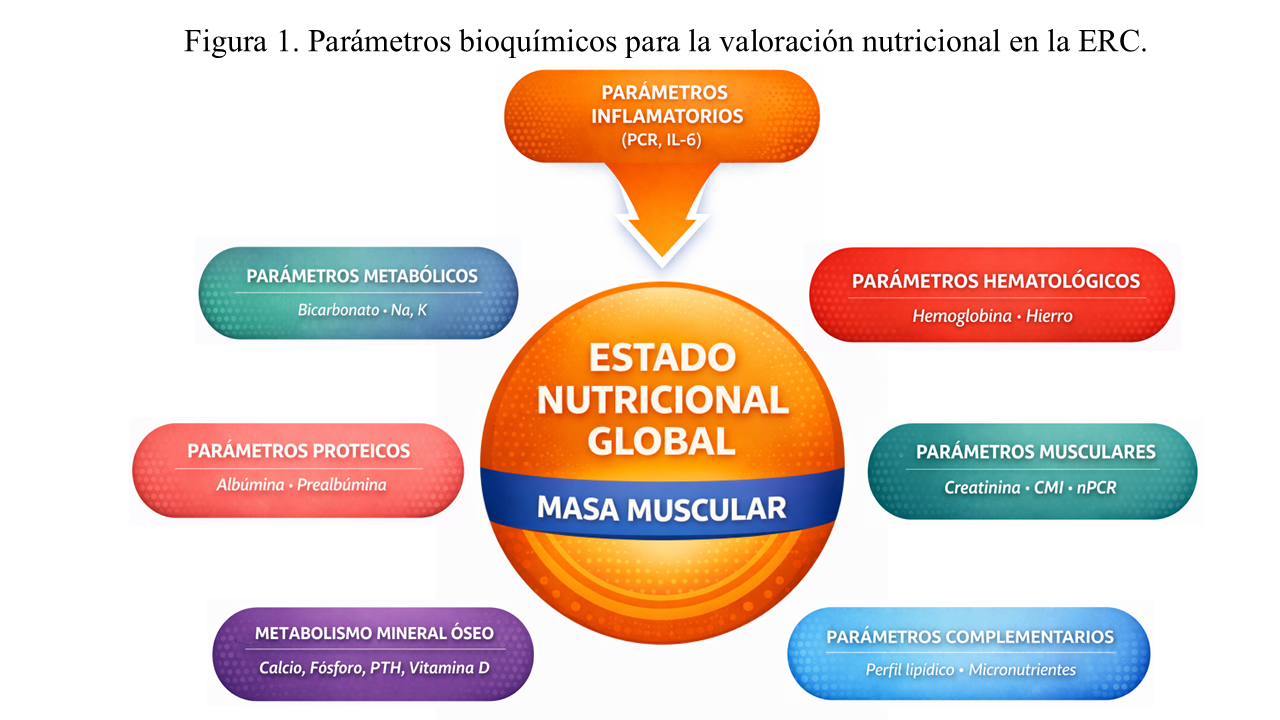
Por ello, las guías clínicas recomiendan evitar el uso de marcadores aislados como "equivalentes" del estado nutricional, y priorizar su lectura en conjunto, valorando las tendencias temporales y su correlación con la situación clínica interpretándose en conjunto con otros datos clínicos y antropométricos [1] [2] (Figura 1).
Parámetros bioquímicos tradicionales específicos y derivados
La albúmina sérica es útil como marcador pronostico, predictor de hospitalización y mortalidad en pacientes con ERC avanzada y en diálisis, pero no debe usarse como único marcador de desnutrición. En la práctica clínica, la determinación de albúmina sérica permite aproximar el riesgo nutricional, presenta una vida media de 20 días. Aunque ampliamente utilizada por su asociación consistente con morbimortalidad, presenta limitaciones como marcador de ingesta debido a su comportamiento como reactante negativo de fase aguda y su sensibilidad a la hemodilución y a la pérdida proteica, especialmente en situaciones como el síndrome nefrótico o la diálisis peritoneal [1] [2] [3]. En este sentido, la evaluación simultánea de PCR resulta esencial para interpretar adecuadamente valores bajos de albúmina, dado que la inflamación es un determinante central del desgaste proteico-energético en la ERC y contribuye al catabolismo muscular y a la reducción de proteínas séricas [3] [4].
La prealbúmina tiene una vida media más corta de 2 a 3 días, una tasa catabólica constante y una concentración plasmática baja, lo que permite reflejar cambios agudos en el estado nutricional, aunque también está influida por inflamación y función hepática [1]. Presenta mayor sensibilidad para detectar cambios agudos en la síntesis proteica en comparación con la albúmina, lo que le convierte en un marcador potencialmente útil para el seguimiento a corto plazo de la respuesta a intervenciones nutricionales, especialmente en pacientes hospitalizados o en situaciones de estrés metabólico.
En pacientes con ERC, la prealbúmina ha demostrado asociación con parámetros nutricionales y pronóstico clínico, incluyendo mortalidad, hospitalización y estado funcional, particularmente en población en diálisis [4]. Al igual que la albúmina, la prealbúmina es un reactante negativo de fase aguda, por lo que sus niveles disminuyen en presencia de inflamación, infección o estrés sistémico, independientemente de la ingesta nutricional. Asimismo, su concentración puede verse afectada por la función hepática, ya que su síntesis es hepática, y por el estado metabólico global del paciente y también por el estado de inflamación. Su utilidad es mayor cuando se analiza en tendencia temporal, más que en valores puntuales, permitiendo identificar cambios dinámicos en el estado nutricional o en la respuesta a intervenciones terapéuticas.
En pacientes en diálisis peritoneal y hemodiálisis, la prealbúmina demostró ser un marcador confiable del estado nutricional, exhibiendo relaciones significativas con ingesta energética y proteica, reservas de grasa y masa corporal magra, con niveles <30mg/dL asociados con mayor riesgo de morbilidad y mortalidad [5]. Los puntos de corte para prealbúmina varían según la población y el contexto clínico. Un estudio retrospectivo y prospectivo con 23,617 pacientes estableció mediante curvas ROC que los valores de corte apropiados son 17 mg/dL para desnutrición y 12 mg/dL para desnutrición severa [6].
La tasa de catabolismo proteico (nPCR o nPNA) estima la ingesta y el estado del metabolismo proteico, siendo útil en pacientes en diálisis y prediálisis en estado estable [1]. Se basa en la producción de nitrógeno ureico derivado del catabolismo de aminoácidos que, en condiciones de equilibrio metabólico, la generación de urea refleja de forma aproximada la ingesta proteica. En pacientes en hemodiálisis, el nPCR se calcula a partir de la generación interdialítica de urea, utilizando modelos cinéticos que tienen en cuenta su distribución y eliminación durante la sesión dialítica. En pacientes sin diálisis puede estimarse a partir de la excreción urinaria de urea en orina de 24 horas, lo que permite una aproximación al catabolismo proteico diario [1] [2]. Las ecuaciones para su estimación están en la (Tabla 1).
Desde el punto de vista clínico, valores de nPCR en torno a 1.0-1.2 g/kg/día en pacientes en hemodiálisis suelen considerarse indicativos de una ingesta proteica adecuada, mientras que valores persistentemente bajos pueden sugerir ingesta insuficiente o malnutrición, y valores elevados pueden reflejar hipercatabolismo o ingesta proteica aumentada. En este sentido, el nPCR se ha incorporado como herramienta de monitorización en múltiples unidades de diálisis, dado su valor para detectar cambios en el balance proteico y orientar intervenciones nutricionales. Este parámetro es útil en el seguimiento, permitiendo detectar tendencias en el metabolismo proteico y evaluar la respuesta a intervenciones dietéticas o terapéuticas. Otra ventaja es que está ampliamente disponible, sin embargo, su interpretación debe realizarse considerando el contexto clínico, con el objetivo de diferenciar entre ingesta insuficiente y aumento del catabolismo endógeno [1] [2] [4].
Otros parámetros bioquímicos relevantes
La hemoglobina, debe incluirse de forma sistemática por la elevada prevalencia de anemia en la ERC y su repercusión sobre la capacidad funcional, la tolerancia al ejercicio y la calidad de vida, elementos estrechamente vinculados al mantenimiento de la masa muscular y a la respuesta a intervenciones nutricionales [7] [8]. En paralelo, la valoración del metabolismo del hierro (ferritina y saturación de transferrina) puede ser necesaria en pacientes con anemia o sospecha de déficit, considerando que la ferritina puede comportarse como reactante de fase aguda y dificultar la interpretación en contextos inflamatorios [8].
Asimismo, el recuento de linfocitos totales ha sido utilizado como marcador indirecto del estado nutricional, reflejando la respuesta inmunitaria; valores <1500 células/mm³ se han asociado con malnutrición, aunque su interpretación está condicionada por la inflamación, infecciones y otras comorbilidades [4].
El ionograma (sodio, potasio y cloro) y el bicarbonato sérico aportan información imprescindible para ajustar la intervención dietética y prevenir complicaciones clínicas asociadas a la ERC. La hiperpotasemia condiciona de forma directa las recomendaciones nutricionales y puede favorecer restricciones excesivas que comprometan la calidad global de la dieta, por lo que su monitorización debe acompañarse de estrategias individualizadas orientadas a preservar la adecuación nutricional [1] [2]. Por su parte, el bicarbonato permite detectar acidosis metabólica, un trastorno frecuente en ERC que se asocia a mayor proteólisis, pérdida de masa muscular y progresión clínica, por lo que su corrección representa un objetivo terapéutico relevante desde el punto de vista metabólico y nutricional [9] [10].
El metabolismo mineral-óseo, (MMO) constituye otro componente esencial en la evaluación bioquímica, debido a su estrecha relación con la dieta, el riesgo cardiovascular y la morbilidad ósea. La monitorización de calcio, fósforo, hormona paratiroidea (PTH) y, fosfatasa alcalina, permite detectar y tratar alteraciones del MMO que condicionan modificaciones dietéticas, necesidad de quelantes y estrategias de suplementación [9]. En este marco, la determinación de 25-OH vitamina D resulta especialmente relevante por su alta prevalencia de déficit en la ERC y su implicación en salud ósea y función muscular, aspectos que influyen de forma directa en el estado nutricional y la fragilidad [11].
La determinación de urea y creatinina mantiene utilidad en la valoración global del paciente al reflejar el grado de uremia y permitir contextualizar síntomas que influyen sobre la ingesta (anorexia, náuseas, disgeusia) y el estado catabólico, si bien no deben considerarse marcadores nutricionales [12] [13]. En pacientes en diálisis, estos parámetros se integran con medidas de adecuación dialítica y, cuando se dispone, con estimaciones indirectas del balance proteico, reforzando el enfoque longitudinal de la valoración [1] [2].
Parámetros complementarios
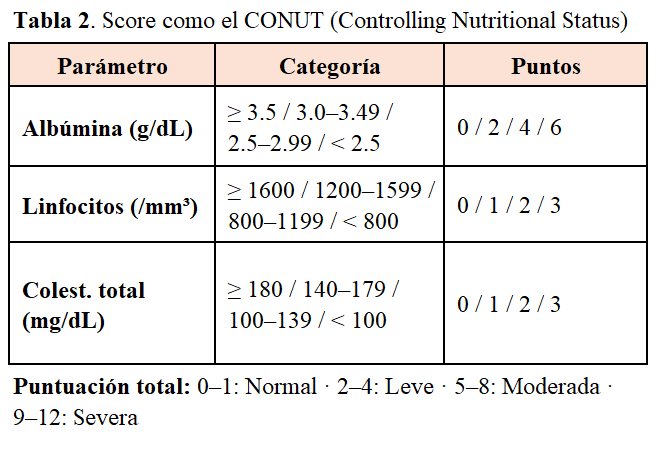
El perfil lipídico, además de su relevancia cardiovascular, puede aportar información adicional en escenarios de inflamación y desgaste, dado que valores bajos de colesterol total se han asociado al síndrome malnutrición-inflamación en ERC avanzada [13]. El colesterol se relaciona con el estado inflamatorio y nutricional de forma inversa. La implementación de scores mejor forma de interpretarse es a través del score como el CONUT (Controlling Nutritional Status) (Tabla 2). Un estudio reciente de pacientes con ERC sin diálisis demostró que tanto el CONUT como el PNI (prognostic nutritional index) mejoraron significativamente la predicción de mortalidad cuando se añadieron a los factores de riesgo cardiovascular convencionales [14].
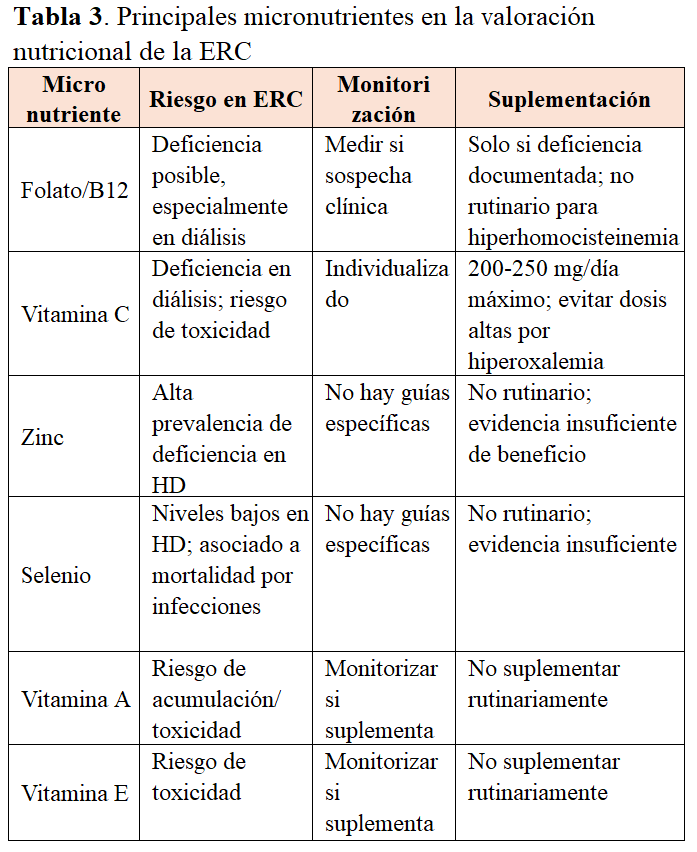
La evaluación de micronutrientes puede considerarse ante dietas restrictivas, síntomas sugestivos o riesgo de déficit, especialmente en pacientes en diálisis o con baja ingesta mantenida [1]. En la (Tabla 3) se resumen los principales micronutrientes.
Parámetros marcadores de masa muscular
La cinética de creatinina se basa en modelos que estiman la producción diaria de creatinina (producto de degradación de la creatina y fosfocreatina del músculo esquelético) a partir de la concentración sérica, la eliminación dialítica y, en algunos casos, la excreción residual urinaria. Este parámetro puede utilizarse para estimar masa muscular en pacientes en diálisis (evidencia 2C), aunque la ingesta alta o baja de proteínas y suplementos de creatina influyen en su precisión. Estudios demuestran que la cinética de creatinina correlaciona con mediciones tradicionales de masa muscular por tomografía computarizada, bioimpedancia y antropometría, y que los niveles de creatinina predicen mortalidad [1].
El índice de músculo de creatinina (CMI), derivado de la relación entre la creatinina sérica y el filtrado glomerular estimado mediante cistatina C (FGe-cys), ha emergido como un marcador prometedor de masa muscular en pacientes con enfermedad renal crónica. Este índice integra un biomarcador dependiente de la masa muscular, como la creatinina, con una estimación de la función renal menos influida por el componente muscular, lo que permite una aproximación más precisa en comparación con la creatinina aislada [15]. Un estudio prospectivo reciente en 2.996 pacientes con ERC sin diálisis demostró que el CMI se asociaba de forma independiente con sarcopenia probable y mortalidad, mostrando además una mayor capacidad discriminativa que otros índices basados en creatinina y cistatina C [16]. Estos hallazgos sugieren que el CMI podría constituir una herramienta útil para la identificación precoz de pérdida de masa muscular y la estratificación pronóstica en la ERC.
Parámetros inflamatorios
La proteína C reactiva (PCR), no es un marcador nutricional directo, sino un marcador de inflamación, con implicaciones profundas en la interpretación del estadio nutricional [2]. Tanto la PCR, como la proteína C ultrasensible (PCRus) e interleucina-6 (IL-6) han ganado relevancia en la valoración nutricional de ERC. Un metaanálisis de 2026 con 81 estudios demostró que niveles elevados de PCR, PCRus y la interleucina 6 (IL-6) se asociaron consistentemente con desenlaces adversos [17]. Además, en el desgaste proteico-energético (DPE) está independientemente asociado con niveles elevados de PCRus [18].
La inflamación crónica es un vínculo crítico entre ERC y enfermedad cardiovascular, con IL-6 y PCRus identificados como biomarcadores pronósticos de riesgo inflamatorio residual [18]. Estudios demuestran que niveles más altos de PCRus se correlacionan con peor estado nutricional, y el Malnutrition Inflammation Score (MIS) ¿7 se asocia con niveles significativamente elevados de IL-6 y PCRus [19]. El MIS que incorpora inflamación mostró superioridad pronóstica comparado con criterios ISRNM y GLIM en pacientes con ERC sin diálisis [19].
Marcadores metabólicos y hormonales
El eje hormona de crecimiento (GH) / factor de crecimiento similar a la insulina tipo 1 (IGF-1) desempeña un papel central en la regulación del anabolismo proteico, la masa muscular y la homeostasis energética. En la enfermedad renal crónica (ERC), este eje se encuentra generando un estado de resistencia anabólica que contribuye al desarrollo de sarcopenia y desgaste proteico-energético [4]. Los pacientes con ERC presentan una disminución de la actividad biológica de IGF-1, especialmente aquellos con desnutrición severa, secundaria a la inflamación crónica, la acidosis metabólica y las alteraciones en las proteínas transportadoras de IGF (IGFBP) [4] [20].
En este contexto, especialmente IGFBP-1 e IGFBP-3, han sido evaluados como posibles biomarcadores del estado nutricional en pacientes con ERC. Estudios observacionales han demostrado que IGF-1 se correlaciona positivamente con parámetros nutricionales como la ingesta proteica estimada y la fuerza de prensión manual, mientras que IGFBP-1 presenta correlaciones inversas con estos mismos parámetros, sugiriendo una relación funcional con el estado anabólico y la masa muscular [21]. Asimismo, IGF-1 e IGFBP-1 muestran asociaciones opuestas con la Evaluación Global Subjetiva (SGA), lo que refuerza su potencial utilidad como indicadores del estado nutricional [21].
La leptina, una adipocina secretada proporcionalmente a la masa grasa, está elevada en ERC debido a reducción del aclaramiento renal. Aunque la hiperleptinemia se asocia con anorexia, caquexia y desgaste proteico-energético en ERC, su utilidad como marcador nutricional es limitada por su papel como posible toxina urémica que contribuye a complicaciones metabólicas [22]. Estudios muestran que niveles elevados de leptina se correlacionan con resistencia a insulina, IGF-1 e IGFBP-3 en pacientes con ERC [23]. La resistina y adiponectina también están elevadas en ERC y se asocian independientemente con menor TFGe y mayor albuminuria.
Conclusión
En conjunto, la selección de parámetros bioquímicos en la valoración nutricional del paciente con ERC debe responder a un enfoque reproducible y complementado según comorbilidades, estadio de la enfermedad renal y modalidad de tratamiento. Su interpretación debe apoyarse en la evidencia disponible y en las guías clínicas, integrando siempre el contexto inflamatorio, el estado de volumen y la evolución temporal, con el objetivo de identificar precozmente el riesgo nutricional y orientar intervenciones individualizadas.
Mensajes clave
La evaluación bioquímica en la ERC debe interpretarse de forma integrada y longitudinal, evitando el uso de marcadores aislados.
Marcadores tradicionales son útiles en el seguimiento, pero requieren una interpretación contextualizada.
Índices integrados y biomarcadores emergentes, mejoran la evaluación del estado nutricional y la masa muscular.
La valoración nutricional en la ERC debe basarse en un enfoque multimodal, integrando parámetros bioquímicos, clínicos, funcionales y de composición corporal.