Intervención Nutricional en el Paciente con Enfermedad Renal Hospitalizado
Índice
1. Introducción
2. Cribado y valoración nutricional del paciente con enfermedad renal hospitalizado
2.1. Pacientes en unidad de hospitalización convencional (estable)
2.2. Pacientes en unidad de agudos o crítico
3. Cálculo de requerimientos en el paciente con enfermedad renal hospitalizado
3.1. Pacientes en estado estable (no crítico)
3.2. Pacientes en estado crítico
3.3. Pacientes con obesidad / sobrepeso
4. Nutrición en insuficiencia renal aguda y técnicas de depuración extrarrenal
4.1. Cambios metabólicos y catabolismo
4.2. Impacto de las técnicas de depuración en pérdidas de nutrientes
4.3. Ajuste de requerimientos en función de la técnica
5. Intervención nutricional
5.1. Aporte de fluidos
5.2. Dieta oral y comorbilidades
5.3. Suplementación nutricional oral
5.4. Nutrición enteral por sonda
5.5. Nutrición parenteral total y nutrición parenteral intradiálisis
6. Vitaminas, micronutrientes y nutrientes específicos
7. Monitorización de la intervención nutricional
8. Recomendaciones al alta hospitalaria
9. Tablas y Figuras
10. Bibliografía
1. Introducción
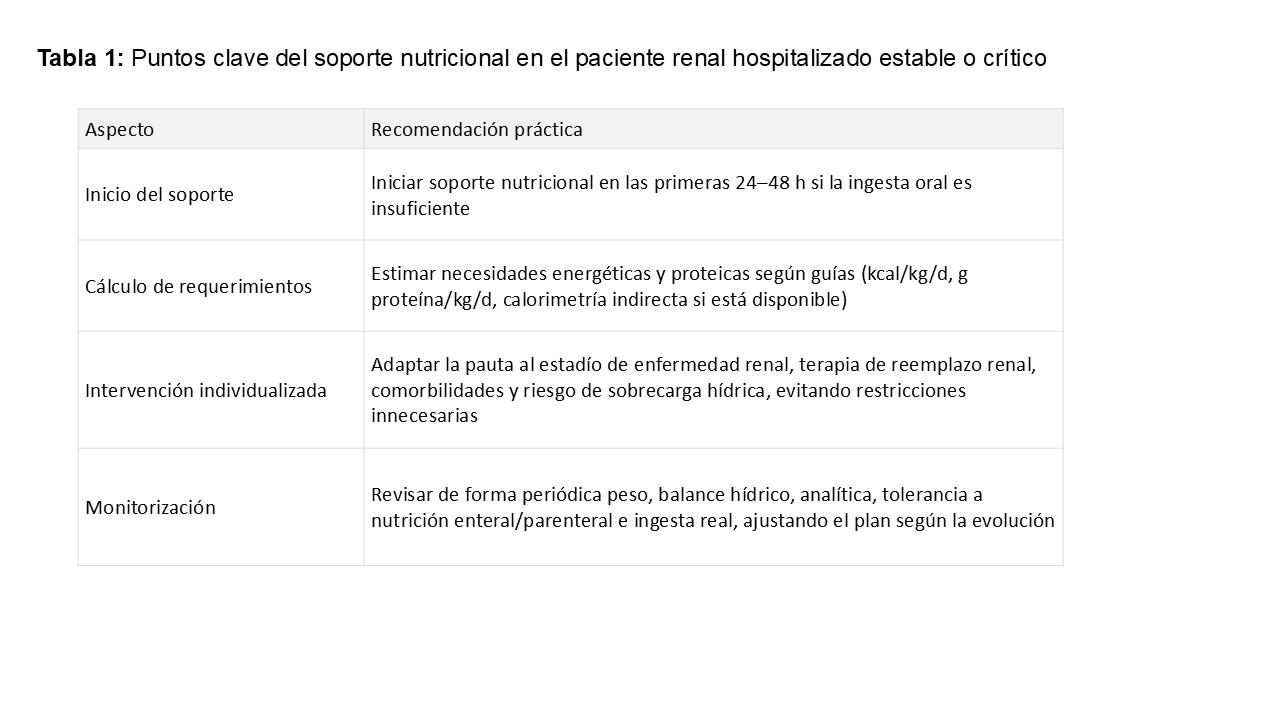
La intervención nutricional en pacientes con enfermedad renal hospitalizados, tanto en situación estable como crítica, es un componente esencial del manejo integral debido a la elevada prevalencia de desnutrición y su asociación con mayor morbimortalidad, infecciones y estancias prolongadas. Factores como el hipercatabolismo, la inflamación crónica, las alteraciones hidroelectrolíticas, las restricciones dietéticas y la propia terapia de reemplazo renal incrementan el riesgo de desgaste proteico- energético, especialmente en la enfermedad renal aguda y en las etapas avanzadas de enfermedad renal crónica. Las guías KDOQI, KDIGO y los documentos ESPEN recomiendan identificar precozmente el riesgo de desnutrición y aplicar estrategias individualizadas que optimicen el aporte calórico- proteico y preserven la masa muscular. Además, revisiones recientes destacan que la terapia médico-nutricional estructurada, con enfoque individualizado, contribuye a controlar hiperfiltración, proteinuria, alteraciones hidroelectrolíticas y acidosis, y a retrasar la progresión de la ERC y la necesidad de TRS [1][2][3][4]. Los puntos clave del soporte nutricional en el paciente renal hospitalizado estable o crítico se encuentran resumidos en la (Tabla 1).
2. Cribado y valoración nutricional del paciente con enfermedad renal hospitalizado
2.1 Paciente en unidad de hospitalización convencional (estable)
En el paciente renal estable ingresado se recomiendan las mismas herramientas de valoración nutricional que en el ámbito ambulatorio (Falta link a capítulo Valoración Nutricional), complementadas con escalas de cribado específicas para paciente hospitalizado, como NRS 2002 y el iNUT Renal que deberían priorizarse en este entorno [2][3][5]. Es importante disponer del peso preingreso o peso seco (en pacientes en diálisis) para interpretar correctamente la evolución ponderal y calcular los requerimientos energéticos y proteicos [2][4].
La valoración completa debe incluir historia dietética, exploración física dirigida a detectar pérdida de masa muscular y tejido adiposo, parámetros antropométricos básicos (perímetro de pantorrilla y dinamometría en brazo dominante) y, cuando sea posible, técnicas como bioimpedancia o ecografía nutricional, siempre teniendo en cuenta las limitaciones derivadas de la sobrehidratación [4][6][7]
2.2 Paciente en unidad de agudos o crítico
En pacientes renales hospitalizados se han validado herramientas específicas como iNUT Renal [6][8][9], junto con escalas generales como NRS 2002, pero en UCI no existe una herramienta de cribado universalmente recomendada, por lo que se aconseja combinar un cribado estructurado con valoración clínica detallada. La antropometría clásica tiene un valor limitado por la sobrecarga de líquido, por lo que adquieren mayor relevancia la bioimpedancia (interpretada con cautela), las técnicas de imagen para masa muscular y grasa (ecografía, TAC, RMN) y la dinamometría en pacientes colaboradores.
En pacientes con lesión renal aguda (LRA) en situación hipercatabólica, las herramientas habituales de diagnóstico de desnutrición-inflamación pueden estar muy alteradas y resultan más útiles durante la fase de recuperación, por lo que la valoración debe apoyarse en la evolución clínica, la función renal, el balance nitrogenado y, cuando esté disponible, la calorimetría indirecta para estimar el gasto energético [2][3][10]. La monitorización debe ser periódica, idealmente diaria en pacientes críticos, integrando exploración física, parámetros analíticos, valoración de ingesta y cambios de peso para ajustar la estrategia nutricional [1][10].
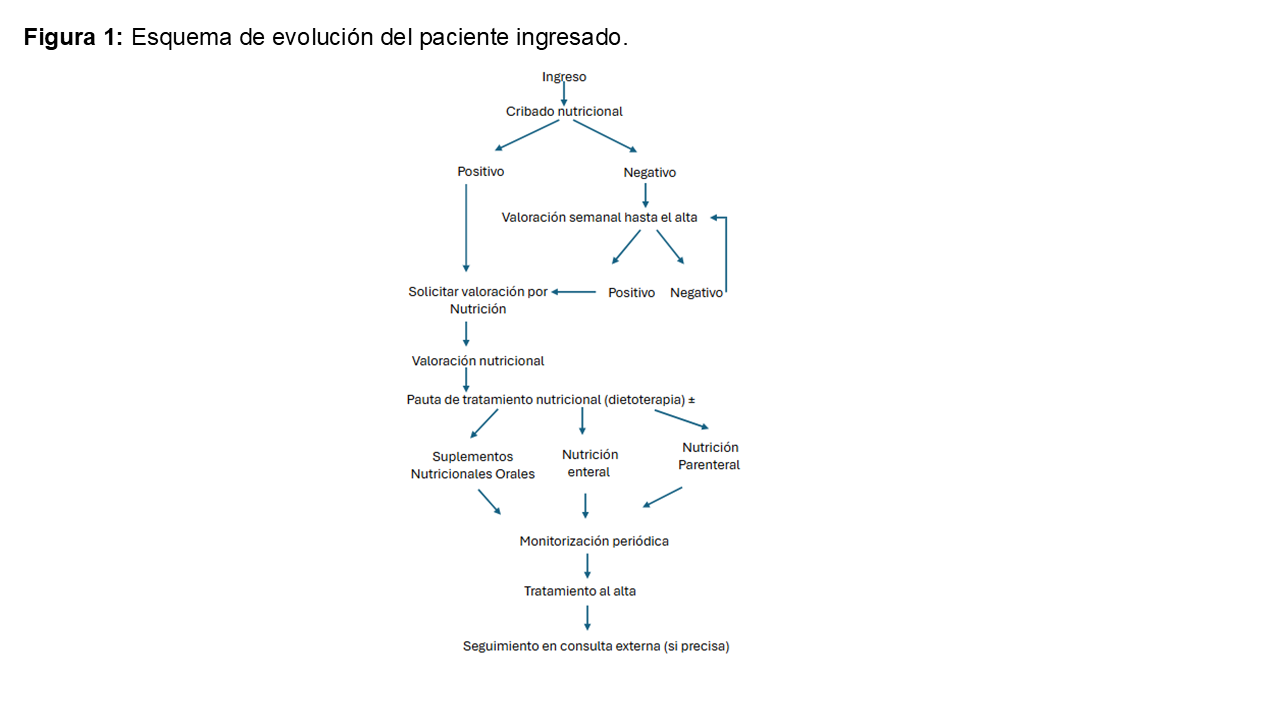
El esquema de evolución de cribado, valoración y tratamiento nutricional del paciente ingresado se resume en la (Figura 1).
3. Cálculo de requerimientos en el paciente con enfermedad renal hospitalizado
3.1. Pacientes en estado estable (no crítico)
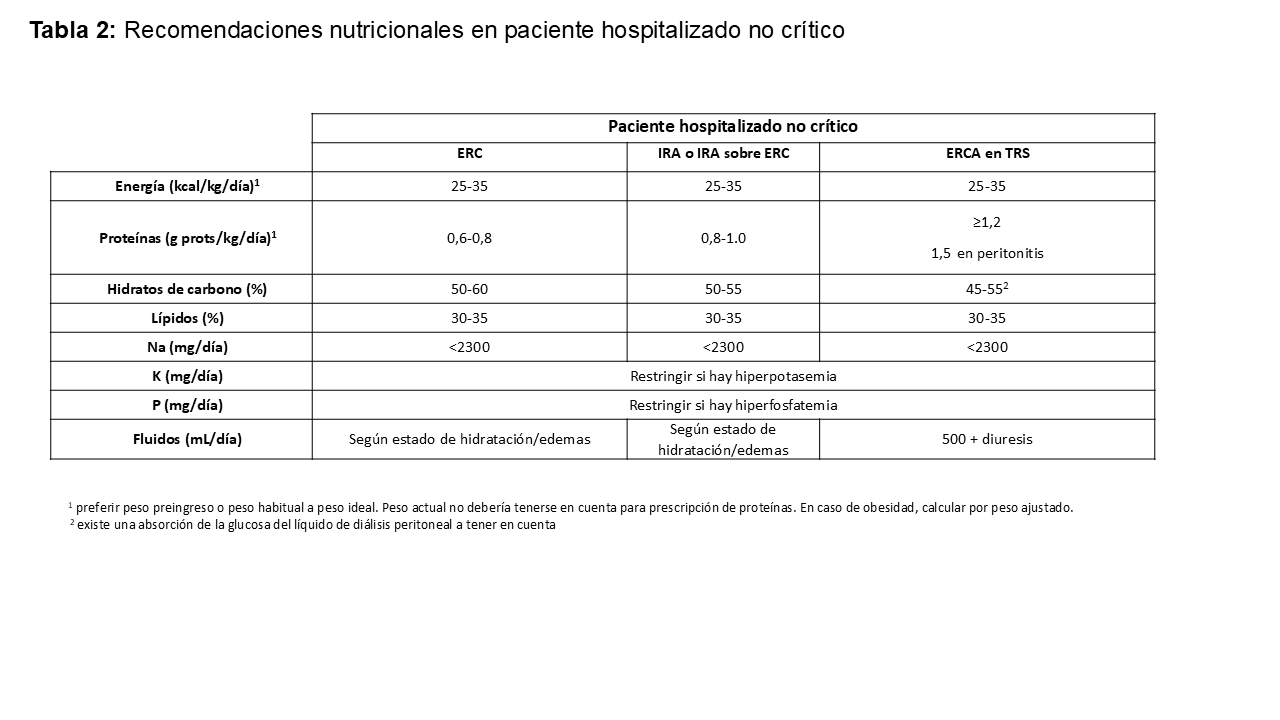
Cuando sea posible, la estimación de requerimientos energéticos debería basarse en calorimetría indirecta, considerada el método de referencia para evitar tanto la sobrealimentación como la infra-alimentación en estos pacientes. En ausencia de este método, puede utilizarse una aproximación de 25-30 kcal/kg/día, priorizando el peso seco en dializados y el último peso sin edemas en pacientes con sobrecarga de líquidos [1][2][3][11]. En pacientes con ERC hospitalizados sin enfermedad aguda grave se recomienda un aporte proteico aproximado de 0,8 g/kg/día en no dializados y 1,2 g/kg/día en pacientes en diálisis, ajustando según la presencia de proteinuria y el estado clínico [1][3][4]. La (Tabla 2) resume estos objetivos para energía, proteínas, hidratos de carbono, lípidos, sodio, potasio, fósforo y fluidos según el estadio de ERC, la presencia de terapia renal sustitutiva (TRS) y la coexistencia de LRA sobre ERC.
En casos de desnutrición grave debe iniciarse con aportes más bajos y aumentarlos de forma progresiva para prevenir el síndrome de realimentación [12].
3.2. Pacientes en estado crítico
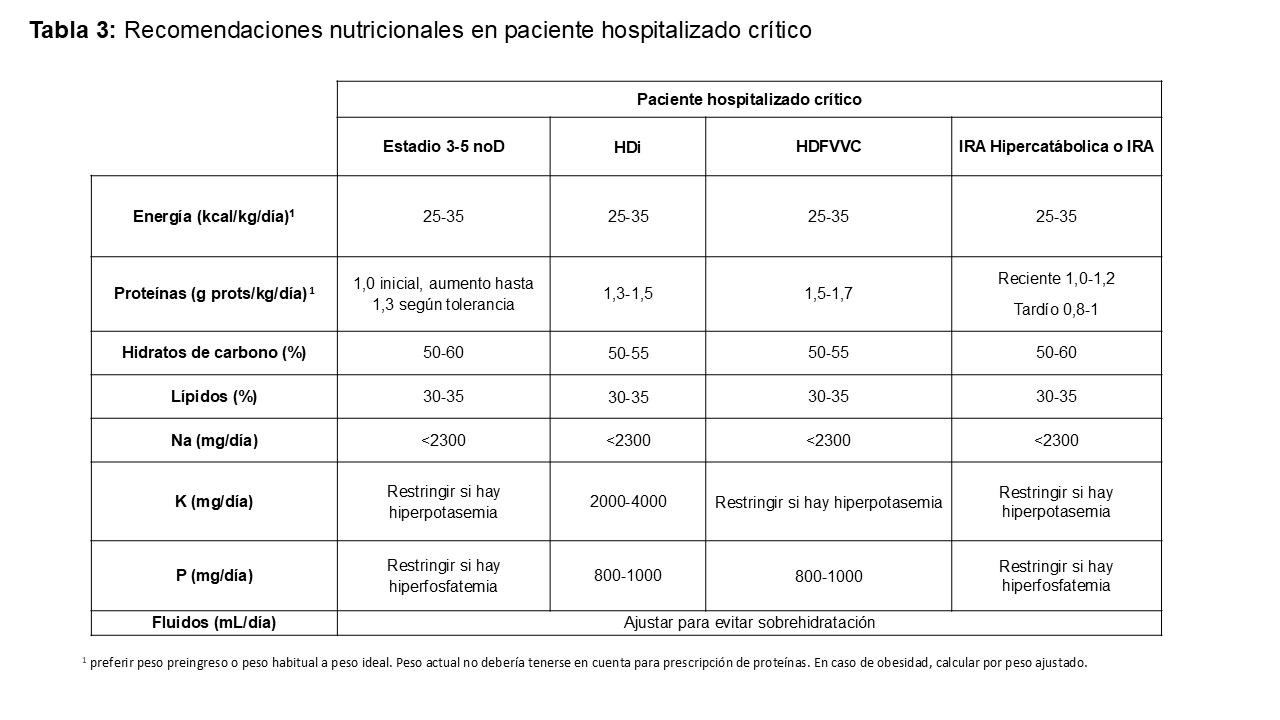
En pacientes críticos con LRA o LRA sobre ERC, el cálculo de requerimientos debe considerar el grado de estrés metabólico, el tipo de soporte renal (tratamiento conservador o depuración extrarrenal) y el riesgo de sobrecarga hídrica (Tabla 3) [1][3][7]. De forma general, se recomiendan 20-30 kcal/kg/día (calorías no proteicas), evitando superar 1,3 veces el metabolismo basal estimado y ajustando según la evolución clínica y, cuando sea posible, la calorimetría indirecta [13].
El aporte proteico en el paciente crítico con terapia extracorpórea suele situarse entre 1-1,5 g/kg/día, pudiendo aumentar hasta 1,7 g/kg/día en situaciones de hipercatabolismo con técnicas continuas de alta intensidad [1][7]. En LRA hipercatabólica sometida a hemofiltración continua de muy alto flujo pueden requerirse aportes proteicos de hasta 2–2,5 g/kg/día para compensar las pérdidas por el filtrado.
3.3. Paciente con obesidad / sobrepeso
En casos de obesidad, el método de elección para el cálculo de requerimientos es asimismo la calorimetría indirecta [13][14]. Cuando esta técnica no está disponible, y siguiendo recomendaciones de guías y documentos de sociedades científicas, pueden utilizarse 11–14 kcal/kg de peso actual/día cuando el IMC está entre 30 y 50 kg/m² y 22–25 kcal/kg de peso ideal/día para IMC mayores de 50 kg/m² en paciente crítico. En cuanto a proteínas, el aporte recomendado es de 1,8–2,5 g/kg de peso ideal/día, individualizando según el grado de estrés metabólico y el tipo de soporte renal [10][14].
En pacientes en estado estable con obesidad la hospitalización no es el momento de pautar dietas hipocalóricas estrictas por el riesgo de sarcopenia; se aconseja utilizar peso ajustado para el cálculo y revisar periódicamente los requerimientos durante el ingreso [15][16].
Como suele haber riesgo de sobrecarga hídrica, especialmente en el compartimento extracelular y con alto riesgo de insuficiencia cardíaca, se recomienda utilizar peso ajustado para el cálculo de los requerimientos y coordinar estrechamente la estrategia nutricional con el plan de ultrafiltración y el balance de fluidos [2]. El grado de catabolismo y la presencia o ausencia de un débito urinario adecuado condicionan el tipo de tratamiento (conservador o con depuración extrarrenal) y, junto con la técnica utilizada, determinan la cuantía y la naturaleza de los aportes de sustratos [17]. En la LRA una sobrecarga de nitrógeno induce la acumulación de productos nitrogenados y puede deteriorar la función renal, por lo que deben evitarse tanto el infra-aporte como la sobrealimentación [18]. Los requerimientos nutricionales concretos se especifican en la (Tabla 2).
4. Nutrición en insuficiencia renal aguda y técnicas de depuración extrarrenal
La LRA es un síndrome caracterizado por un rápido fallo de la función renal, con acúmulo de productos nitrogenados, disregulación del metabolismo hidroelectrolítico y el equilibrio ácido-base [19][20]. Puede aparecer como fracaso aislado o en el seno del síndrome de disfunción orgánica múltiple. Su incidencia es baja en la población general, pero aparece en el 7 % de los pacientes hospitalizados y en el 28-35 % [21] de los ingresados en las unidades de cuidados intensivos, con aumento de la mortalidad hospitalaria. El fallo grave de la función renal (que suele entenderse como pérdida de la tasa de filtración glomerular) no sólo afecta el volumen corporal, los electrolitos y el ácido-base, sino que también induce cambios globales en el "medio interno", junto con alteraciones específicas en los metabolismos de proteínas, aminoácidos, carbohidratos y lípidos. Además, ejerce una acción proinflamatoria y tiene un impacto negativo en el sistema antioxidante.
4.1. Cambios metabólicos y catabolismo
Los cambios metabólicos en estos pacientes también están determinados por la enfermedad subyacente y/o las comorbilidades, por la disfunción de otros órganos, así como por la modalidad e intensidad de la terapia de reemplazo renal. Las anomalías metabólicas específicas importantes asociadas a la LRA son [22]:
• catabolismo proteico
• alteración del metabolismo de aminoácidos específicos
• resistencia periférica a la insulina
• reducción de la lipólisis y alteración de la eliminación de grasas
• agotamiento de los sistemas antioxidantes
• inducción de un estado proinflamatorio
• inmunodeficiencia
Los pacientes con enfermedad renal deben someterse a una valoración del estado nutricional, que incluya valoración de la inflamación, con el desarrollo de un plan de cuidado nutricional siendo el catabolismo proteico el sello metabólico distintivo de la insuficiencia renal aguda, especialmente en el entorno de la UCI [2].
El tratamiento nutricional debe instaurarse en cuanto se detecta la insuficiencia renal aguda, para limitar el catabolismo proteico y la malnutrición, reducir el número de complicaciones y mejorar el estado nutricional con vistas a posibles necesidades futuras, como el tratamiento renal con diálisis. El término de «fracaso renal hipercatabólico» fue acuñado por Parsons y cols. en 1961 para describir un tipo de fallo renal agudo caracterizado por elevaciones diarias de urea sérica superiores a 60 mg/dl, que se acompañaba de alta mortalidad y precisaba sesiones diarias de hemodiálisis [23]. Es el más frecuente en el paciente crítico con síndrome inflamatorio sistémico o con disfunción multiorgánica.
Teóricamente, un adecuado aporte nutricional debería mejorar la evolución de la insuficiencia renal aguda. En individuos sanos, el aporte de proteínas y de aminoácidos incrementa la tasa de filtración glomerular y el flujo renal, con mayor diuresis y natriuresis, con la participación de IGF-1, glucagón, prostaglandinas y óxido nítrico. No obstante, en la insuficiencia renal aguda, la sobrecarga de nitrógeno induce la acumulación de restos nitrogenados y puede deteriorar la función renal. Aumenta el flujo a las nefronas no lesionadas, con elevación de las presiones transcapilares y mayor grado de esclerosis [17].
4.2. Impacto de las técnicas de depuración en pérdidas de nutrientes
La hemodiálisis provoca la pérdida de unos 6 g de aminoácidos y 28 g de glucosa por sesión. La diálisis peritoneal produce una pérdida de 9 g/día de proteínas y 4 g/día de aminoácidos, cifras que se incrementan notablemente en caso de peritonitis o irritación peritoneal [24].
En lo referente a las pérdidas nitrogenadas a través del hemofiltrado, tanto los estudios en pacientes críticos con hemofiltración arteriovenosa continua [25] como los dedicados a la hemofiltración veno-venosa continua [26] y la hemodiafiltración veno-venosa continua [27]) confirman pérdidas similares de aminoácidos (10 13 g/día), que pueden ser fácilmente compensadas por los altos aportes nitrogenados recomendados para los pacientes con elevado grado de estrés.
En un estudio encaminado a determinar los aportes de nitrógeno y calorías más eficaces para conseguir mejores balances nitrogenados en la insuficiencia renal aguda tratado con hemofiltración veno-venosa continua, se recomiendan aportes de 2 g de aminoácidos/kg/día, con una relación calorías/nitrógeno baja [28][29]. Este estudio se realizó antes de que se utilizaran las técnicas de muy alto flujo.
4.3. Ajuste de requerimientos en función de la técnica
Debe administrarse una tercera parte de las calorías no proteicas como lípidos, y dos terceras partes como hidratos de carbono. Con respecto a la ingesta proteica se mantiene la controversia, siendo las recomendaciones hasta 0,8-1 g/kg/día en la terapia sin diálisis, 1-1,5 g/kg/día en el tratamiento extracorpóreo, y hasta 1,7 g/kg/día en estados hipercatabólicos con tratamiento sustitutivo renal [2].
5. Intervención nutricional
El tratamiento nutricional debe iniciarse en cuanto se detecta la desnutrición o su riesgo, ya que permite reducir el catabolismo proteico y se asocia a menos complicaciones y a una estancia hospitalaria más corta [30]. Además, es fundamental disminuir el riesgo de desnutrición asociada al ingreso, favorecido por los ayunos prolongados motivados por pruebas diagnósticas o intervenciones quirúrgicas, minimizando dichos ayunos y restableciendo la dieta oral o la nutrición enteral lo antes posible para evitar la desnutrición nosocomial [2].
5.1. Aporte de fluidos
La cantidad de líquidos que consume el paciente renal ingresado es primordial para el control de la sobrecarga hídrica y la aparición de edemas o insuficiencia cardiaca congestiva, por lo que se recomienda monitorizar el peso de forma regular (idealmente diaria) y registrar la ingesta y el balance hídrico [31]. Además de controlar la cantidad total de líquidos (agua, café, leche, zumos, gelatinas, sopas, cremas, platos caldosos, helados), es importante recordar que muchos alimentos aportan agua “oculta” (pasta y arroz muy cocidos, verduras hervidas mal escurridas), por lo que conviene priorizar cocciones secas (horno, plancha, salteado, microondas) y alimentos al dente [2][30].
En pacientes con ERC avanzada o en diálisis se debe individualizar la restricción hídrica en función del balance de volumen, la diuresis y las indicaciones del equipo médico; en UCI el objetivo será mantener la euvolemia coordinando la estrategia de fluidos, nutrición y ultrafiltración, especialmente cuando se utiliza nutrición parenteral [2][10].
En el paciente renal ingresado, la restricción de sal debe reflejarse directamente en la pauta hospitalaria, evitando dietas “generales” con alto contenido en sodio y priorizando dietas hiposódicas ajustadas al balance de volumen, la presión arterial y la diuresis. Es importante que el equipo médico y de enfermería conozca los límites de sodio prescritos (habitualmente en el rango de 2-2,3g de sodio/día –equivalente a 5-6g de sal/día– salvo indicación contraria) y evite añadir sal en bandejas, ya que pueden agravar la sobrecarga hídrica y la hipertensión durante el ingreso [31].
5.2. Dieta oral y comorbilidades
Las recomendaciones actuales en el paciente renal hospitalizado priorizan un patrón alimentario saludable y variado, similar a la dieta mediterránea, ajustando alimentos y nutrientes a la situación renal, comorbilidades y resultados analíticos. En las personas con ERC se aconseja evitar restricciones dietéticas excesivas e indiscriminadas, individualizando los límites de potasio, fósforo, sodio y proteínas según el estadio de ERC y la presencia de hiperpotasemia o hiperfosfatemia, ya que pautas demasiado estrictas pueden empeorar la ingesta y favorecer la malnutrición [2][3][31][32].
En pacientes con ERC y diabetes ingresados, es prioritario un buen control glucémico; en insuficiencia renal aguda o ERC con fallo renal hospitalizados se aceptan rangos de glucemia algo más amplios (por ejemplo, 140-180 mg/dl) para reducir el riesgo de hipoglucemias durante el ingreso, siguiendo las recomendaciones de nutrición hospitalaria y en UCI [33][34]. En personas con obesidad la pérdida de peso rápida no es prioritaria durante el ingreso por el riesgo de sarcopenia y desgaste proteico-energético; se recomienda centrarse en mejorar la calidad de la dieta, el control de sodio y el perfil cardio-metabólico, preferentemente con patrones de tipo mediterráneo o basados en vegetales [15][35]. En pacientes con disfagia, se debe adaptar la textura de alimentos y líquidos a la viscosidad segura para la deglución, valorado de manera individual, garantizando que la modificación de textura no reduzca el aporte calórico-proteico [30][36].
5.3. Suplementación nutricional oral
La suplementación nutricional oral es la primera opción de soporte nutricional cuando la ingesta habitual no cubre los requerimientos (por ejemplo, ingesta <75% de lo requerido durante una semana o <50% durante ≥3 días en el hospital) a pesar de las adaptaciones dietéticas [3][4][29][36]. Las fórmulas deben seleccionarse según las necesidades nutricionales del paciente, las comorbilidades (como diabetes) y la situación clínica (por ejemplo, control de electrolitos), siendo especialmente útiles las fórmulas específicas para ERC cuando existe sobrecarga hídrica o alteraciones séricas de potasio y fósforo.
Se recomienda fraccionar las tomas y administrarlas separadas de las comidas principales o después de ellas para no reducir la ingesta de alimentos, considerándolas un complemento y no un sustituto de la dieta. Es importante tener en cuenta las preferencias organolépticas y, si aparecen molestias digestivas por la osmolaridad, ajustar la pauta (volumen por toma o tipo de fórmula) para favorecer la tolerancia [30]. A nivel nacional -España-, la financiación de estos productos tras el alta depende del diagnóstico y de la normativa vigente (p. ej., BOEA200616212 y BOEA202412290), por lo que conviene planificar el tratamiento valorando la continuidad asistencial [38][39].
5.4. Nutrición enteral por sonda
La nutrición enteral por sonda es la modalidad de elección cuando el sistema digestivo es funcionante pero la vía oral no permite cubrir los requerimientos, ya sea por disfagia, reducción marcada de la ingesta o necesidad de soporte continuo (por ejemplo, en UCI) [3][40]. Mantiene el trofismo intestinal y se prefiere a la nutrición parenteral siempre que no haya contraindicaciones. Existen múltiples fórmulas nutricionales y se seleccionará la más adecuada según función renal, estado hemodinámico, electrolitos y objetivos de líquidos. Para periodos cortos (días o semanas) se prefieren sondas nasogástricas o nasoyeyunales, mientras que para soportes prolongados o cuando la vía nasoentérica no es viable, se recomiendan gastrostomías o yeyunostomías [30].
En pacientes críticos, incluidas las personas con LRA o ERC con fallo renal, se recomienda iniciar la nutrición enteral precozmente –idealmente dentro de las primeras 24-48 horas– siempre que no exista contraindicación, ajustando el volumen al balance hídrico y al riesgo de intolerancia digestiva [10]. La elección de la fórmula (estándar, específica para ERC, hipercalórica, etc.) debe basarse en el estado hemodinámico, la función renal, la presencia de hiperkalemia o hiperfosfatemia.
5.5. Nutrición parenteral total y nutrición parenteral intradiálisis
La nutrición parenteral total (NPT) debe considerarse cuando el tracto digestivo es inaccesible o no funcionante, o cuando, pese a la dieta oral, los suplementos y/o la nutrición enteral, no se alcanzan los requerimientos nutricionales. En pacientes renales críticos con LRA o ERC con fallo renal en UCI, se aplican las mismas indicaciones generales de NPT que en otros pacientes críticos, vigilando de forma estrecha el balance hídrico, los electrolitos (especialmente fósforo y magnesio) y el riesgo de síndrome de realimentación [24].
La nutrición parenteral intradiálisis (NPID) es una opción de soporte nutricional parcial en pacientes con ERC en hemodiálisis que presentan desnutrición o riesgo nutricional y no alcanzan los requerimientos con dieta y suplementos orales, o no toleran la nutrición enteral. Su administración se realiza durante la sesión de hemodiálisis, por lo que debe considerarse un complemento y no un sustituto de otros aportes; su uso generalizado antes de intentar suplementos orales no se considera justificado. Los consensos específicos recomiendan reservar la NPID para pacientes con criterios claros de desnutrición o ingesta inadecuada prolongada y siempre dentro de un plan de cuidado nutricional estructurado con objetivos definidos y reevaluación periódica [41][42][43].
Siguiendo las guías ESPEN de nutrición hospitalaria y renal, la indicación global de soporte nutricional (suplementos orales, nutrición enteral o parenteral) se basa en el cribado nutricional, la presencia de desnutrición o riesgo alto y la imposibilidad de cubrir al menos el 70% de los requerimientos por vía oral [3][30].
6. Vitaminas, micronutrientes y nutrientes específicos
Los pacientes con enfermedad renal hospitalizados presentan con frecuencia déficits de vitaminas hidrosolubles (especialmente complejo B y vitamina C) debido a restricciones dietéticas, anorexia, pérdidas dialíticas y procesos inflamatorios, por lo que suele recomendarse una suplementación diaria adaptada a la función renal y a la técnica de diálisis, cuando exista [44][45]. En cambio, las vitaminas liposolubles (A, E, K) y oligoelementos como aluminio pueden acumularse, por lo que no se aconseja una suplementación indiscriminada y deben evitarse preparados con dosis elevadas de vitamina A o formulaciones no específicas para paciente renal [2][4].
El hierro, el ácido fólico y la vitamina B12 deben monitorizarse de forma periódica, especialmente en pacientes con anemia tratada con agentes estimulantes de la eritropoyesis, ajustando la suplementación oral o intravenosa según guías de anemia en ERC [46][47]. En cuanto al calcio, fósforo y vitamina D, es imprescindible coordinar la intervención nutricional con el tratamiento nefrológico (quelantes de fósforo, análogos de vitamina D, calcimiméticos), individualizando la restricción de fósforo dietético y la dosis de vitamina D para prevenir tanto la desnutrición como las complicaciones óseo-minerales [1].
En pacientes críticos con LRA o ERC con fallo renal, se recomienda vigilar estrechamente magnesio, fósforo y tiamina, dado el mayor riesgo de síndrome de realimentación y de depleción por diuréticos o terapias de reemplazo renal continuas, suplementando cuando los valores sean bajos o existan factores de riesgo elevados [2][48]. En pacientes en hemodiálisis con enfermedad renal crónica, la suplementación con ácidos grasos omega 3 puede mejorar algunos marcadores del perfil cardiovascular y del estado inflamatorio, por lo que su uso puede considerarse de forma individualizada como terapia complementaria, aunque no forma parte del soporte nutricional estándar y requiere una valoración caso por caso [49][50].
7. Monitorización tras la intervención nutricional
La monitorización del paciente renal hospitalizado tras el inicio del tratamiento nutricional debe ser sistemática y estructurada, tanto en el paciente estable como en el crítico. En el paciente estable se recomienda controlar la evolución del peso al menos semanalmente (preferiblemente diario cuando haya riesgo de sobrecarga hídrica), registrar la presencia de edemas y utilizar, cuando sea posible, medidas antropométricas complementarias (pliegues cutáneos, perímetro de pantorrilla), bioimpedancia, ecografía nutricional y dinamometría para valorar cambios en la composición corporal y la fuerza muscular [2][30].
La monitorización analítica debe incluir parámetros séricos y, cuando proceda, urinarios (función renal, sodio, potasio, fósforo, magnesio, glucemia, marcadores de inflamación), con una periodicidad adaptada a la situación clínica, siendo razonable una reevaluación cada 3–5 días en pacientes con riesgo nutricional moderado-alto. Es importante valorar periódicamente el apetito y la ingesta real mediante registros dietéticos o estimaciones sistemáticas, para decidir si es preciso ajustar la pauta: modificar textura, fraccionar comidas, introducir o aumentar suplementos orales o cambiar a nutrición enteral/parenteral si la ingesta sigue siendo insuficiente.
En el paciente crítico, la monitorización debe ser más estrecha, con control diario del balance hídrico, el peso –si es posible con báscula cama–, parámetros hemodinámicos y complicaciones relacionadas con la nutrición enteral –intolerancia digestiva, riesgo de aspiración– o parenteral –alteraciones metabólicas, complicaciones infecciosas–. Herramientas como la bioimpedancia, la ecografía muscular y la dinamometría, cuando el estado del paciente lo permite, ayudan a valorar la evolución de la masa muscular en el tiempo, complementando la información clínica y analítica [10].
8. Recomendaciones al alta hospitalaria
Para consolidar la recuperación del estado nutricional y mantener los resultados obtenidos durante el ingreso, se recomienda entregar por escrito y explicar de forma individualizada las recomendaciones dietético-nutricionales en el momento del alta hospitalaria. Estos consejos deben tener en cuenta el estadio de la enfermedad renal, las comorbilidades (diabetes, obesidad, enfermedad cardiovascular), la situación funcional y el entorno social, e idealmente, incluir cantidades orientativas de alimentos y ejemplos de menús o combinaciones de comidas que faciliten la adherencia [2][4].
La necesidad de suplementación nutricional oral a domicilio debe valorarse antes del alta, revisando el riesgo nutricional, la evolución del peso y la capacidad de mantener una ingesta adecuada; en caso de requerirla, se seleccionará la fórmula más adecuada y se informará al paciente sobre la pauta y la duración prevista. La financiación de estos productos depende de la normativa vigente y del diagnóstico que favorece la desnutrición (p. Ej. En territorio español: amiloidosis, desnutrición en lista de trasplante renal y, desde 2024, hemodiálisis), así como de los acuerdos específicos de cada comunidad autónoma [38][39].
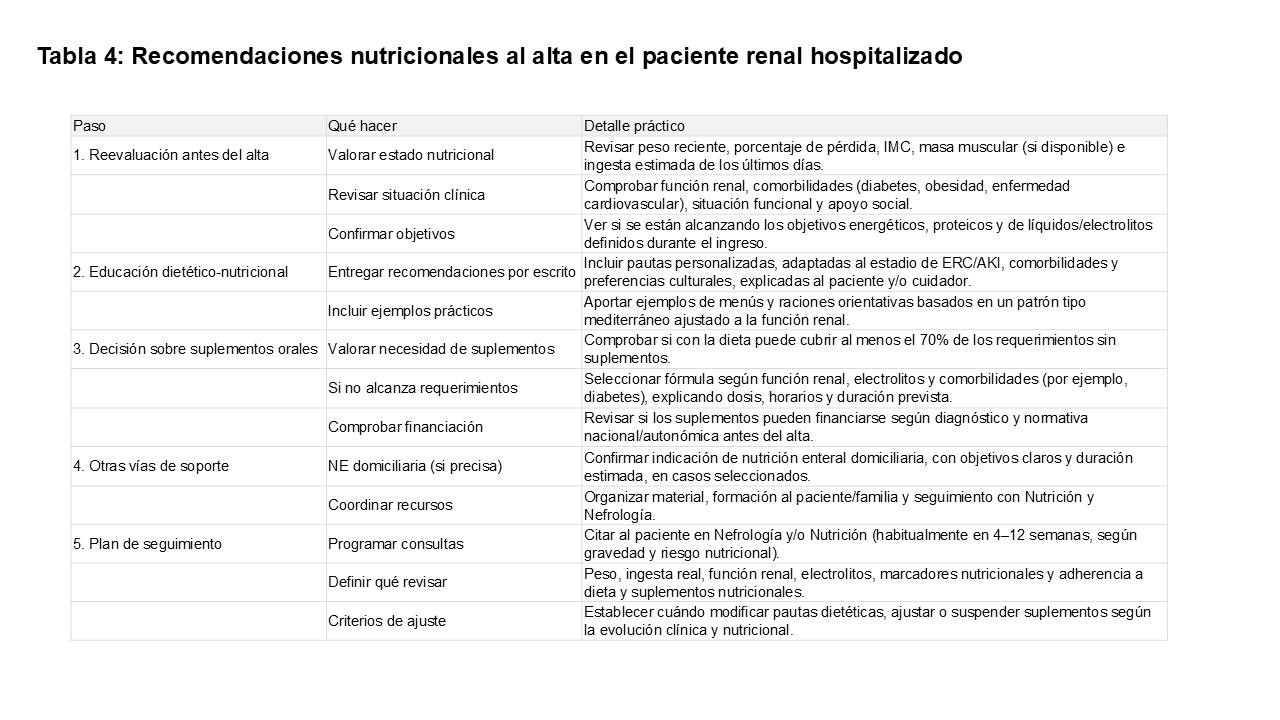
Se aconseja organizar un seguimiento en consultas externas (Nefrología y/o Nutrición) para revisar periódicamente el estado nutricional, la función renal y la adherencia al tratamiento dietético, ajustando la pauta o suspendiendo suplementos cuando la situación mejore [2][30]. En pacientes críticos dados de alta de UCI, debe garantizarse la continuidad del plan nutricional (oral, enteral o parenteral domiciliaria cuando esté indicada), con objetivos claros, criterios de reevaluación y coordinación entre niveles asistenciales [10]. (Tabla 4)