Nefropatía asociada a Gammapatías Monoclonales
Palabras clave
nefropatía por cadenas ligeras, riñon del mieloma, cadenas pesadas, amiloidosis
INTRODUCIÓN
La gammapatía monoclonal o paraproteinemia es una entidad clínica caracterizada por la presencia de cantidades elevadas de inmunoglobulinas o fracciones de las mismas monoclonales en sangre (paraproteína o proteína M), sintetizadas por clonas de linfocitos B maduros o de células plasmáticas [1] [2].
Los procesos hematológicos linfo o plasmoproliferativos asociados a la producción de paraproteínas pueden ser diversos, y se resumen en la (Tabla 1). Los criterios diagnósticos de la mayoría de estas entidades se han ido actualizando y consensuando en los últimos años [3] [4] [5], y se basan tanto en las características morfológicas e inmunofenotípicas de las clonas celulares implicadas como en el tipo y cantidad de la paraproteína sintetizada y en su repercusión a nivel de órgano diana (Tabla 2).
El tipo de paraproteína sintetizada puede ser una inmunoglobulina completa o cadenas ligeras o pesadas libres, o una combinación de ambas, tanto como estructuras enteras o como fragmentos truncados más o menos grandes de las mismas.
En condiciones normales, durante el proceso de síntesis de inmunoglobulinas se producen cadenas ligeras en exceso, las cuales se pueden detectar en suero en cantidades reducidas. Debido a su pequeño tamaño (la cadena κ, monomérica, tiene unos 22.5 kD y la cadena λ, predominantemente dimérica, unos 45 kD) son filtradas libremente en el glomérulo y reabsorbidas y metabolizadas en su totalidad a nivel del túbulo contorneado proximal. Esta relación directa entre el riñón y las cadenas ligeras explica que éste sea uno de los órganos con mayor frecuencia afectado en las gammapatías monoclonales, sobretodo cuando la paraproteína está compuesta predominantemente por cadenas ligeras.
La demostración de daño renal directamente relacionado con la paraproteína tiene una gran trascendencia clínica, terapéutica y pronóstica en las gammapatías monoclonales, por lo que durante el estudio y seguimiento de las mismas debe monitorizarse de forma sistemática la función renal y la proteinuria (añadiendo albuminuria y sedimento urinario en caso de alteración de los anteriores). La sospecha de nefropatía debe abordarse desde un punto de vista multidisciplinar, con estrecha colaboración entre el nefrólogo y el hematólogo.
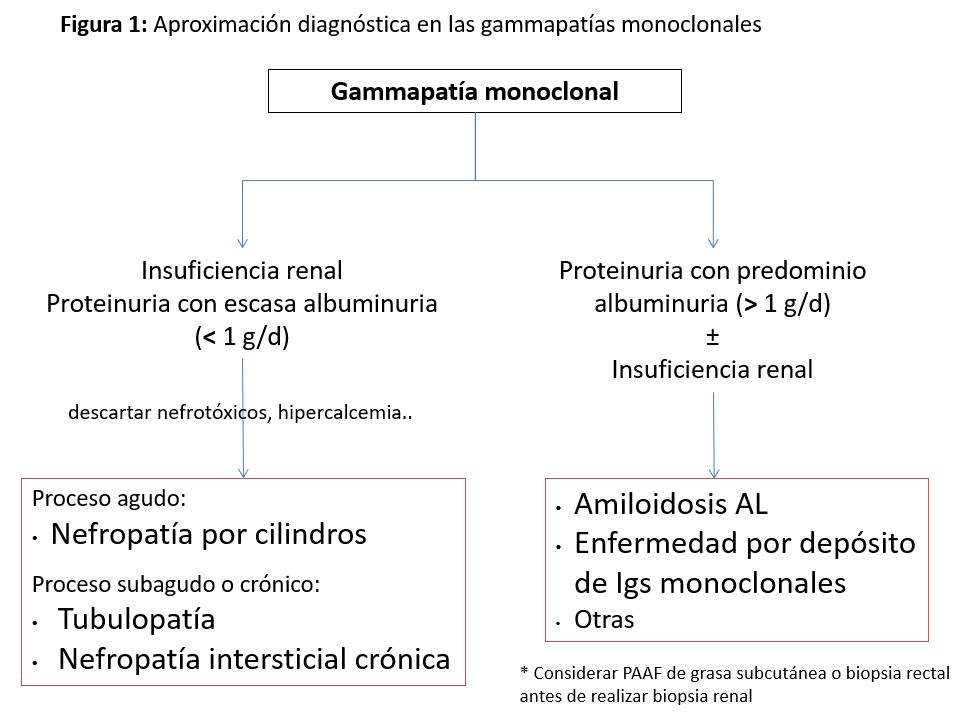
El daño renal causado por la paraproteína puede presentarse de múltiples formas: como fracaso renal agudo, insuficiencia renal crónica, disfunción tubular, o proteinuria ya sea asintomática o como síndrome nefrótico o nefrítico. La forma de presentación dependerá del substrato patológico desarrollado, el cual a su vez estará condicionado por el tipo y cantidad de paraproteína sintetizada. A menudo las manifestaciones clínicas no permiten establecer un diagnóstico específico de la lesión renal subyacente, por lo que es necesaria en la mayoría de los casos la biopsia renal. Este procedimiento, bajo control ecográfico, se ha demostrado seguro en este tipo de pacientes [6]. La (Figura 1) puede ayudar a una primera aproximación diagnóstica en función de la presentación clínica. No debemos olvidar que, aunque no sea la norma, pueden coexistir diferentes patrones patológicos en un mismo paciente con paraproteinemia.
Debemos tener en cuenta que la nefropatía asociada a las gammapatías monoclonales puede ser la primera manifestación de las mismas, y que no es extraño que se llegue al diagnóstico del trastorno hematológico a partir de los hallazgos obtenidos en el estudio de la nefropatía.
MÉTODOS BÁSICOS DE ESTUDIO DE UNA PARAPROTEÍNA:
Ante la sospecha de una gammapatía monoclonal se debe confirmar y caracterizar la paraproteína, e identificar la clona celular productora.
La principal prueba para documentar la paraproteína es el proteinograma o electroforesis en suero. Ante la detección de una banda monoclonal la inmunofijación permitirá caracterizar su composición. En caso de sospecha de la presencia de una paraproteína en orina la inmunofijación en orina aporta mayor rendimiento sin tener que realizar previamente un proteinograma urinario. Sin embargo, para la detección de cadenas ligeras la electroforesis y la inmunofijación son poco sensibles (el límite de sensibilidad de la inmunofijación ronda los 100-150 mg/L) y no proporcionan resultados cuantitativos. En la actualidad se dispone de métodos de inmunoensayo (inmunonefelometría) que permiten detectar y cuantificar incluso cantidades pequeñas de cadenas ligeras libres κ y λ de forma independiente (nivel de sensibilidad hasta 2-4 mg/L), permitiendo calcular así la ratio entre ambas (κ/λ) [7] [8]. Estos estudios tienen una especial utilidad para detectar y cuantificar las cadenas ligeras libres monoclonales en suero en casos en los cuales existe una alta sospecha de un proceso linfo o plasmoproliferativo sin alteraciones en la electroforesis ni en la inmunofijación, como puede pasar en casos oligosecretores de mieloma múltiple, de amiloidosis sistémica AL o de enfermedad por depósito de cadenas ligeras [9] [10].
Tras la detección de la paraproteína en suero u orina es necesaria la identificación de la clona celular responsable de la misma mediante la realización de un aspirado de médula ósea o biopsia ósea. En caso de normalidad de la misma deberá extenderse el estudio para descartar plasmocitoma o linfoma mediante una TAC toracoabdominal o un PET-TAC 18-FDG, y obtención de muestra para estudio histológico de la adenopatía o zona patológica siempre que sea posible.
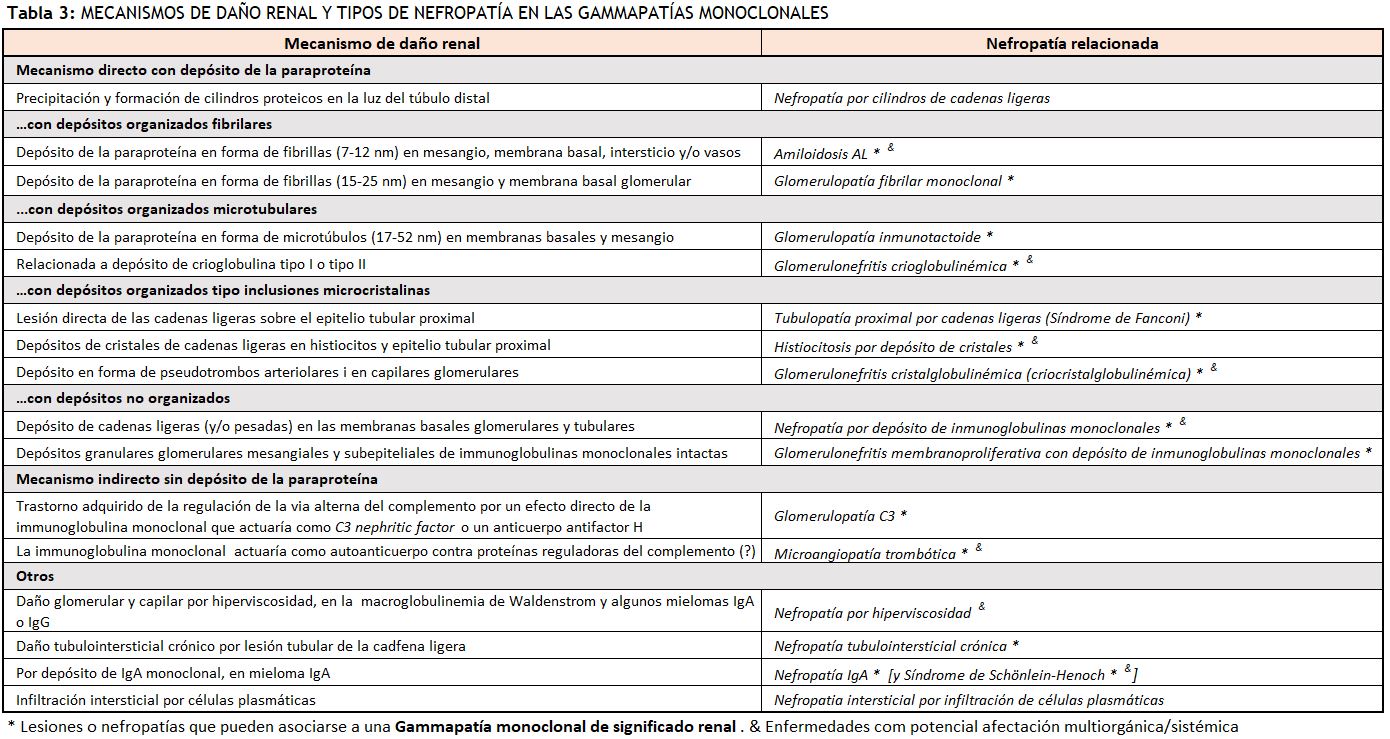
MECANISMOS DE DAÑO RENAL Y TIPOS DE NEFROPATÍA EN LAS GAMMAPATÍAS MONOCLONALES.
El tipo de repercusión sistémica en las gammapatías monoclonales, y concretamente en el riñón los mecanismos de daño y compartimento afectado, dependerá de la cantidad de paraproteína sintetizada así como también, en gran parte, del tipo de inmunoglobulina y de su estructura y características morfológicas y fisicoquímicas [11] [12]. Por ejemplo, a nivel renal las cadenas ligeras κ están implicadas de forma predominante en el desarrollo de tubulopatía proximal (concretamente el subgrupo Vκ1) [13] y de enfermedad por depósitos de cadenas ligeras (principalmente el subgrupo Vκ4) [14], mientras que en los casos de amiloidosis AL predomina la participación de las cadenas ligeras λ (subgrupo Vλ6) [15].
Los mecanismos de daño renal son diversos, y determinan la expresión clinicopatológica de cada una de las nefropatías específicas [2] [16] [17] (Tabla 3).
Nefropatía por cilindros de cadenas ligeras. Riñón de mieloma
Se produce por la precipitación de las cadenas ligeras a nivel intratubular. Las cadenas ligeras sobreproducidas, filtradas en el glomérulo, sobrepasan la capacidad de reabsorción y metabolismo de las células tubulares proximales llegando en grandes cantidades a nivel del asa ascendente de Henle y túbulo distal donde, en determinadas circunstancias y tras unirse a la proteína de Tamm-Horsfall, precipitan en forma de cilindros. Estos cilindros dificultan el flujo tubular y generan una reacción inflamatoria local y del área intersticial circundante [18]. El resultado es el desarrollo de insuficiencia renal de evolución variable con diuresis conservada, pero que puede ser severa y de rápida instauración, incluso oligoanúrica. El fracaso renal a menudo se desencadena por factores precipitantes como situaciones de depleción de volumen de cualquier causa, hipercalcemia, la toma de diuréticos o de antiinflamatorios no esteroideos, o la realización de exploraciones con contrastes iodados endovenosos.
Esta entidad se asocia principalmente al mieloma múltiple (clásicamente se la ha denominado "riñón de mieloma"), aunque puede presentarse en otras enfermedades linfoproliferativas con alta masa tumoral y siempre que se sinteticen grandes cantidades de cadenas ligeras. La insuficiencia renal se suele acompañar de la clínica de la enfermedad hematológica subyacente, si bien no es raro que la manifestación renal sea la primera en generar la consulta. Es por ello que ante todo fracaso renal agudo o subagudo acompañado de anemia con un sedimento normal y proteinuria importante sin o escasa albuminuria debe estudiarse la existencia de una paraproteína, tanto en sangre como en orina. La cuantificación de cadenas ligeras libres en suero puede ser de gran ayuda. La probabilidad de nefropatía por cilindros de cadenas ligeras es muy alta ante un fracaso renal agudo con una concentración elevada de cadenas ligeras libres en suero (mayor o igual a 500 mg/L) [19] [20] [21]. El diagnóstico definitivo se obtiene con la realización de una biopsia renal, siempre que la situación clínica del paciente lo permita, no solo para establecer el diagnóstico de certeza sino también como elemento pronóstico en función del daño crónico ya instaurado. El número y extensión de los cilindros tubulares y el daño crónico tubulointersticial se han correlacionado de forma inversa con la recuperación de la función renal [22].
Histológicamente se caracteriza por un daño tubular difuso, tanto a nivel del túbulo proximal como distal, con la presencia característica en los túbulos distales de cilindros intratubulares de tinción eosinofílica, irregulares, angulados y con líneas de fractura, a menudo generando a su alrededor una reacción inflamatoria tipo cuerpo extraño con monocitos y células gigantes multinucleadas. En el intersticio aparece un grado variable de infiltrado linfocitario, mientras que los glomérulos y los vasos no están afectados. Los cilindros intratubulares suelen ser positivos en la inmunofluorescencia para la cadena ligera monoclonal κ o λ implicada.
El tratamiento se fundamenta, tras la corrección del factor desencadenante si lo hubiera, en la reducción de la carga de paraproteína, mediante el bloqueo de la síntesis con tratamiento quimioterápico. Como tratamiento adyuvante se puede valorar la utilización de técnicas de eliminación de cadenas ligeras libres circulantes con diversos métodos de depuración extrarenal [23] [24]. La rapidez en la actuación es un factor determinante, ya que la demora en el diagnóstico y en la instauración de tratamiento se relaciona con un peor pronóstico renal [25].
El tratamiento quimioterápico de primera línea se basa en pautas de alta eficacia y rapidez de acción con dosis altas de dexametasona y bortezomib, habitualmente en forma de triple terapia asociado a fármacos no nefrotóxicos y que puedan administrarse de forma segura en situación de insuficiencia renal (talidomida o ciclofosfamida principalmente) [21] [26]. Sin embargo un reciente estudio randomizado cuestiona la utilidad de añadir un tercer fármaco (ciclofosfamida) en pacientes sin requerimiento de diálisis, no pudiendo demostrar una mayor eficacia en términos de recuperación de la función renal y en cambio con un mayor riesgo de efectos secundarios, principalmente infecciosos, en estos pacientes habitualmente frágiles [27].
El bortezomib, un inhidor del proteasoma, ha demostrado en diversos estudios ser eficaz en controlar la actividad del mieloma y mejorar la función renal [28] [29] [30] [31]. Además de su efecto quimioterápico sobre las células plasmáticas, se postula que pueda tener un efecto de bloqueo sobre el efecto proinflamatorio y profibrótico que generan las cadenas ligeras a nivel tubular [32]. Actúa de forma rápida, y su farmacocinética no se ve afectada en caso de insuficiencia renal. En los pacientes con requerimiento de tratamiento renal sustitutivo su administración es segura, aunque al ser una molécula de pequeño tamaño se recomienda su administración tras la sesión de hemodiálisis [33].
Los fármacos inmunomoduladores talidomina y lenalidomida también se consideran fármacos eficaces en el tratamiento del mieloma múltiple con afectación renal, ya sea asociados a bortezomib y dosis altas de dexametasona, o como alternativa cuando el bortezomib no se pueda administrar. La lenalidomida, sin embargo, ve limitado su uso en esta situación debido a su eliminación renal, requiriendo ajuste de dosis [34]. La pomalidomida, un inmunomodulador de tercera generación, no tiene excreción renal significativa por lo que se postula como una droga potencialmente utilizable en esta indicación.
Actualmente existen nuevos fármacos cuya farmacocinética no se ve alterada de forma significativa en insuficiencia renal, como los nuevos inhibidores del proteasoma, carfilzomib e ixazomib, que han emergido como alternativas a bortezomib, panobinostat o anticuerpos monoclonales como daratumumab (anti-CD38) o elotuzumab (anti-SLAMF7). Sin embargo, hoy por hoy aún la experiencia es muy limitada en este tipo de pacientes.
En los casos que se haya alcanzado al menos una remisión parcial con el tratamiento de inducción, y que por edad y situación clínica sea factible, debe plantearse la posibilidad de trasplante de progenitores hematopoyéticos.
La eliminación de las cadenas ligeras mediante técnicas de depuración extrarrenal se ha considerado una opción terapéutica desde hace tiempo, con una sólida base teórica, siempre asociada a la quimioterapia. La plasmaféresis ha sido la técnica clásicamente utilizada, estando actualmente en discusión su efectividad tras los diversos estudios realizados con resultados discordantes [35] [36] [37], manteniendo su indicación dentro de la categoría II según la Sociedad Americana de Aféresis, con un grado de evidencia 2B, y principalmente en los casos de estados de hiperviscosidad en mieloma múltiple y macroglobulinemia de Waldenström, dentro de la categoría I con un grado de evidencia 1B [38]. Se consideraba que podría quedar definitivamente desplazada por la aparición en la última década de las nuevas membranas de diálisis "high cut-off" con un tamaño de poro lo suficientemente grande (aproximadamente 50 kd) como para permitir el aclaramiento de las cadenas ligeras [39] [40], con unos estudios iniciales prometedores [41]. Dos estudios controlados europeos recientes utilizando membranas de diálisis "high cut-off" en pacientes con fracaso renal agudo por nefropatía por cilindros de cadenas ligeras (confirmada con biopsia renal) con requerimiento de diálisis y bajo tratamiento concomitante con quimioterapia basada en bortezomib, han aportado sin embargo, resultados poco concluyentes y que no permiten afianzar esta terapia de forma sólida y definitiva. El estudio MYRE [42] comparó pautas de tratamiento sustitutivo renal intensiva (sesiones de 5 horas, durante 8 días consecutivos), un grupo con un filtro high cut-off (Theralite®, 2.1 m2, Gambro) otro grupo con un filtro de alto flujo convencional. No se consiguió el objetivo primario de recuperación de función renal a los 3 meses, sin diferencias entre los dos grupos, aunque sí se obtuvo una diferencia significativa en el grupo con el filtro de high cut-off en cuanto a recuperación de función renal a más largo plazo, a los 6 (56.5 vs 35.4%) y 12 meses (60.9 vs 37.5%), sin diferencias de mortalidad a los 12 meses de seguimiento. El estudio EuLITE [43] comparó pautas con sesiones de hemodiálisis más largas, de 8 horas, durante 8 días consecutivos seguidas de sesiones a días alternos, un grupo con dos filtros high cut-off en serie (HCO 1100®, 1.1 m2, Baxter-Gambro) y otro grupo con un filtro de alto flujo convencional. No se consiguió el objetivo primario de recuperación de función renal a los 3 meses, sin diferencias entre los dos grupos, ni tampoco a más largo plazo, y en cambio se observó una mayor incidencia de infecciones pulmonares a los 3 meses y una menor supervivencia global a los 2 años de seguimiento en los pacientes tratados con el filtro de high cut-off. Estos resultados permiten confirmar que las terapias de reemplazo renal con membranas "high cutt-off" mejoran la depuración de cadenas ligeras patogénicas en los pacientes con insuficiencia renal aguda por nefropatía por cilindros, y aunque según el estudio MYRE parece que puedan favorecer la recuperación de la función renal más allá de los 3 meses de seguimiento, no han demostrado que mejoren la supervivencia del paciente a largo plazo, con potencial mayor riesgo de infecciones. La utilización de otras membranas, como el polimetilmetaclilato (PMMA) [44], o de otras técnicas de depuración extrarenal, como la hemodiafiltración con regeneración de ultrafiltrado [45] [46], ambas con un efecto adsortivo relevante sobre las cadenas ligeras libres en suero, han mostrado eficacia variable en términos de reducción de la carga de cadenas ligeras en sangre en pacientes con requerimiento concomitante de tratamiento sustitutivo renal, sin pérdida significativa de albúmina, aunque carecen de estudios randomizados que sustenten su utilización en términos de recuperación de función renal o de supervivencia del paciente.
Sea como sea lo que está claro es que el tratamiento debe ser precoz ya que la probabilidad de recuperación de la función renal depende, además del grado de daño crónico ya instaurado en el riñón, de la cantidad y rapidez en conseguir la reducción de la concentración plasmática de cadenas ligeras [47].
Enfermedad por depósito de inmunoglobulinas monoclonales (cadenas ligeras, cadenas pesadas o cadenas ligeras y pesadas).
Se caracteriza por el depósito a nivel de las membranas basales de diversos tejidos de inmunoglobulinas monoclonales, tanto enteras como subunidades de las mismas, habitualmente cadenas ligeras (enfermedad por depósito de cadenas ligeras) aunque también pesadas (enfermedad por depósito de cadenas pesadas) o una combinación de ligeras y pesadas.
Suele aparecer en casos de mieloma múltiple, aunque también en casos aparentemente más indolentes como la gammapatia monoclonal de significado incierto [48]. La cadena ligera principalmente implicada suele ser la κ [14].
Debe considerarse una enfermedad sistémica ya que los depósitos de cadena ligera pueden detectarse además de en el riñón, donde aparecen prácticamente siempre, en órganos como el hígado, el corazón, el bazo... dando una clínica muy variable, desde asintomático hasta disfunciones severas de los órganos afectados [48]. A nivel renal se manifiesta clínicamente como proteinuria, habitualmente de rango nefrótico, e insuficiencia renal en grado variable, con microhematuria aproximadamente en 2/3 de los pacientes. En los casos de enfermedad por depósito de cadenas pesadas la hipocomplementemia es frecuente.
Por la presentación clínica el diagnóstico diferencial debe realizarse principalmente con la amiloidosis AL.
Para el diagnóstico es imprescindible la biopsia renal donde se observa el característico patrón de glomerulopatía esclerosante nodular y engrosamiento de la membrana basal tubular, rojo congo negativo, con una inmunofluorescencia positiva lineal en membranas basales glomerulares y principalmente tubulares (dato imprescindible para el diagnóstico) para una cadena ligera monotípica, o una cadena pesada o una cadena pesada y una ligera específicas. A nivel ultraestructural se observan depósitos electrondensos granulares puntiformes en la membrana basal tubular y a lo largo de la membrana basal glomerular, y depósitos finamente granulares "no fibrilares" en el mesangio [49].
Las lesiones esclerosantes renales se deben a la capacidad del depósito de cadena ligera de estimular la síntesis de matriz extracelular por parte de la células adyacentes, principalmente las mesangiales [50].
Las lesiones pueden ser reversibles [51] siempre que se consiga reducir la inmunoglobulina monoclonal. Por ello en los pacientes que su situación clínica lo permita debe intentarse el tratamiento quimioterápico, con pautas basadas en bortezomib [52], o plantear el trasplante de precursores hematopoyéticos siempre en estrecha colaboración con el hematólogo [53] [54].
Amiloidosis AL
Es una enfermedad sistémica de depósito extracelular en diversos órganos de material fibrilar compuesto por cadenas ligeras. La cadena ligera mayoritariamente implicada es la λ, en concreto del subgrupo Vλ6 [15], dato que ayuda a realizar el diagnóstico diferencial con la enfermedad por depósito de inmunoglobulinas monoclonales, donde predomina la k.
La amiloidosis AL (antiguamente llamada amiloidosis primaria) puede aparecer en el seno de una gammapatía monoclonal ya conocida, mieloma múltiple sintomático o quiescente o gammapatía monoclonal de significado incierto, aunque es frecuente que sea la primera manifestación, detectando la presencia de banda monoclonal en sangre u orina posteriormente en su estudio. Aproximadamente en un 10% de casos no se detecta banda monoclonal en sangre u orina mediante electroforesis o inmunofijación. En estos casos es útil la determinación de cadenas ligeras libres en suero, con mayor sensibilidad para detectar pequeñas elevaciones monoclonales no detectables por otros métodos [55].
Las manifestaciones clínicas son muy parecidas a las de la enfermedad por depósito de inmunoglobulinas monoclonales, con diversas potenciales manifestaciones sistémicas (miocardiopatía, polineuropatía..), siendo principalmente la afectación cardíaca la que determina el pronóstico. A nivel renal la proteinuria de origen glomerular es la principal manifestación, pudiendo llegar a desarrollar síndrome nefrótico florido, e insuficiencia renal de grado variable. Característicamente los riñones presentan un tamaño aumentado en las pruebas de imagen.
Ante la sospecha de esta entidad, y debido a un potencial mayor riesgo de sangrado ante pruebas cruentas como una biopsia renal, se aconseja el estudio de muestras histológicas de fácil acceso, como la punción-aspiración con aguja fina o biopsia de grasa subcutánea, la biopsia de glándulas salivares o la biopsia de mucosa rectal, en búsqueda del material de depósito rojo congo positivo. Este aspecto hoy en día está en discusión, con series que no encuentran mayor riesgo de sangrado en estos pacientes al realizar una biopsia renal bajo control ecográfico si no presentan alteraciones importantes de la hemostasia [56].
En el estudio anatomopatológico renal destacan los depósitos glomerulares mesangiales y en membranas basales de un material amorfo, acelular y eosinófilo, que no tiñe con la tinción de PAS y sí en cambio presenta la característica tinción rojo congo positiva con birrefringencia verde manzana a la luz polarizada. Los depósitos pueden también estar presentes en los vasos y en los túbulos e intersticio, e incluso en ocasiones predominando en estos compartimentos. La inmunofluorescencia es importante para poder discernir el tipo de amiloide, siendo aquí los depósitos positivos para la cadena ligera monoclonal implicada, habitualmente λ. En el estudio ultraestructural los depósitos están compuestos de fibrillas pequeñas, de 8-12 nm de diámetro de distribución desordenada.
Ante el diagnóstico de amiloidosis AL siempre debe realizarse estudio de gammapatía monoclonal si no es conocida previamente, buscando la paraproteína en sangre y orina, utilizando entre otros la cuantificación de cadenas ligeras libres en suero.
El tratamiento de la amiloidosis AL debe focalizarse en erradicar la discrasia de células plasmáticas subyacente. Solamente bloqueando la síntesis de la paraproteína con una respuesta hematológica completa y sostenida en el tiempo se puede prever una mejoría de la afectación y disfunción de los diferentes órganos afectados. El tratamiento quimioterápico debe plantearse en estrecha relación multidisciplinar con el hematólogo. En los pacientes jóvenes ( < 65 años) con un estado general conservado y sin contraindicaciones para el mismo debe plantearse la posibilidad de trasplante de precursores hematopoyéticos tras un tratamiento quimioterápico intenso. En los pacientes no candidatos a trasplante se han ensayado diversas pautas de quimioterapia con altas dosis de dexametasona junto a melfalan o ciclofosfamida i/o bortezomib. Actualmente las pautas con bortezomib junto a ciclofosfamida y dexametasona se consideran las de primera opción, principalmente en pacientes con insuficiencia renal [57]. Pautas con inmunomoduladores (lenalidomida y pomalidomida) o daratumumab se reservan para los casos refractarios o recidivantes [58].
Tubulopatía proximal (Síndrome de Fanconi) por cadenas ligeras.
Se caracteriza por daño tubular proximal con depósitos de cristales intracelulares de cadenas ligeras. Las cadenas ligeras son predominantemente de tipo κ, aunque también hay casos descritos con cadenas ligeras λ. Su específica patogenicidad viene determinada por la secuencia de aminoácidos de la cadena ligera y las características fisicoquímicas resultantes que le confieren una particular resistencia a las proteasas de los lisosomas de las células tubulares proximales [13]. Las células tubulares proximales, en su intento de reabsorber y metabolizar las cadenas ligeras filtradas son incapaces de degradarlas correctamente y en consecuencia se acumulan, cristalizan y precipitan en el citoplasma provocando su daño y disfunción.
Es una complicación poco frecuente, presentándose la mayor parte de los casos en pacientes con mieloma múltiple, a menudo en los de poca expresión clínica (asintomático o quiescente), aunque también pueden aparecer en casos de gammapatia monoclonal de significado incierto o de otros procesos linfoproliferativos con paraproteinemia.
La clínica suele ser inicialmente poco expresiva, y no es raro que se diagnostique de forma tardía tras años de evolución en un estudio de disfunción renal, o de astenia o dolores óseos, relacionados más con las alteraciones metabólicas que provoca que con la enfermedad hematológica de base. Su cortejo biológico es el propio del síndrome de Fanconi adquirido, no siempre completo, con hiperaminoacidúria, glucosuria normoglicémica, hiperfosfaturia con hipofosfatemia, hiperuricosuria con hipofosfatemia, hipokaliemia, acidosis metabólica tubular tipo II y disfunción renal en grado variable, habitualmente leve o moderada. La hipofosfatemia mantenida a lo largo del tiempo provoca que muchos de estos pacientes desarrollen osteomalacia, manifestando síntomas propios de la misma como dolores óseos difusos y fracturas recurrentes, siendo en ocasiones la primera manifestación de la enfermedad y que lleva al diagnóstico de la enfermedad plasmo o linfoproliferativa tras el estudio de la misma.
A nivel histológico en la microscopia óptica a menudo aparecen lesiones inespecíficas de daño tubular, siendo necesario para el diagnóstico el estudio ultraestructural para observar los cristales intracelulares romboidales o trapezoidales de cadenas ligeras en las células tubulares proximales [59].
El tratamiento y manejo de esta entidad es controvertido. Depende en gran manera de la entidad de la enfermedad hematológica de base y de la repercusión clínica del trastorno metabólico provocado. Sin duda la solución definitiva para controlar el daño tubular continuo es controlar la síntesis de paraproteína y evitar su llegada en grandes cantidades al túbulo proximal. Reduciendo la carga de cadena ligera que llega al túbulo proximal este puede regenerarse y mejorar el síndrome de Fanconi. En casos leves, sin insuficiencia renal y sin manifestaciones clínicas importantes secundarias a los trastornos metabólicos y óseos, se considera que su evolución suele ser indolente, y que no justifica un tratamiento quimioterápico [60]. En aquellos casos en que el trastorno plasmoproliferativo no cumple criterios de tratamiento, el desarrollo de insuficiencia renal o clínica derivada de las alteraciones metabólicas, como osteomalacia sintomática, deben considerarse "lesión de órgano diana" y por lo tanto deberían ser criterios de tratamiento quimioterápico, siempre sopesando en cada paciente el riesgo-beneficio del mismo [61].
Las alteraciones metabólicas que aparecen se tratan con suplementación de bicarbonato, potasio y fósforo según requerimientos, y si la osteomalacia está instaurada puede ser de utilidad la adición de vitamina D. Debe tenerse en cuenta que, a pesar de un tratamiento eficaz sobre le enfermedad hematológica, la recuperación de los trastornos metabólicos suele ser muy lenta.
GAMMAPATIA MONOCLONAL DE SIGNIFICADO RENAL
Desde el punto de vista estrictamente hematológico, solamente tienen indicación de tratamiento aquellos procesos linfo o plasmoproliferativos con criterios de malignidad (mieloma múltiple sintomático, macroglobulinemia de Waldenström o leucemia linfocítica crónica / linfoma linfocítico de célula pequeña). Aunque estas enfermedades son las que habitualmente se relacionan a cargas mayores de paraproteínas y a mayor riesgo de lesión renal, la nefropatía relacionada a paraproteína puede aparecer también en aquellos casos de procesos hematológicamente benignos o asintomáticos.
Para poder identificar y englobar estos casos se acuñó el término "gammapatía monoclonal de significado renal" [62]. Se define como aquellos procesos linfoproliferativos monoclonales de célula B o plasmoproliferativos de bajo grado o indolentes, que no requieren de entrada tratamiento desde el punto de vista hematológico, pero que son responsables de lesión renal a través de la síntesis de paraproteína. Dentro de estas entidades se incluyen la gammapatía monoclonal de significado incierto (no-IgM, IgM o de cadena ligera), mieloma quiescente o smouldering, macroglobulinèmia de Waldenström indolente o smouldering, linfocitosis B monoclonal y linfomas de bajo grado.
El espectro de nefropatías englobadas dentro de este concepto es amplio y se pueden clasificar según el tipo i características del depósito o del mecanismo patogénico de la paraproteína [63] [64] (Tabla 3). La mayoría de las nefropatías descritas anteriormente pueden presentarse como una gammapatía monoclonal de significado renal, excepto la nefropatía por cilindros de cadenas ligeras, que forma parte de los eventos definitorios de mieloma múltiple sintomático, igual como pasa con las lesiones por hiperviscosidad, que definen lesión de órgano diana en la macroglobulinemia de Wäldenstrom.
Estos procesos requieren ser abordados desde el punto de vista terapéutico con un tratamiento dirigido a controlar la clona celular y la producción de la paraproteína para evitar una progresiva evolución de la nefropatía a enfermedad renal terminal [61].