Diuréticos
Los diuréticos son uno de los grupos farmacológicos más utilizados en la práctica clínica habitual. El conocimiento de sus peculiaridades farmacocinéticas y farmacodinámicas, que además pueden verse modificadas en las situaciones clínicas donde su uso está indicado, resultan fundamentales para conseguir un uso eficiente de los mismos. En los próximos párrafos, se describirán aquellos puntos críticos que pueden limitar su efecto clínico, y cuyo reconocimiento puede ayudar a optimizar su uso.
Finalmente hablaremos brevemente de otras indicaciones de los diuréticos, como en el tratamiento de la hipertensión o la formación de litiasis.
Características Farmacocinéticas y Farmacodinámicas de los diuréticos.
Farmacocinética
Todos los diuréticos, a excepción de la espironolactona, eplerenona y de un nuevo bloqueante mineralcorticoide no esteroideo (la finerenona, actualmente en evaluación en ensayos clínicos), necesitan alcanzar el espacio luminal para actuar. El filtrado glomerular tiene un papel menor en la llegada de diuréticos dentro del compartimento urinario, por su extensa unión de los diuréticos a proteínas.
Los diuréticos llegan al espacio luminal utilizando unos transportadores orgánicos ácidos (diuréticos de asa, tiacida y acetazolamida) o básicos (amiloride y triamterene) presentes en el túbulo contorneado proximal, en concreto en su segmento S2. Por ello en situación de acidosis metabólica (por uremia o por otros motivos) o en pacientes con hiperuricemia, la entrada al túbulo de los diuréticos de asa, tiacídicos y acetazolamida puede estar disminuida por competencia con presencia de moléculas ácidas. Paralelamente en situación de alcalosis metabólica la llegada de triamterene o amiloride puede estar limitada. Algunos fármacos, como los AINEs, algunos antibióticos o antivirales pueden interaccionar con estos transportadores y reducir la entrada de los diuréticos al interior del túbulo.
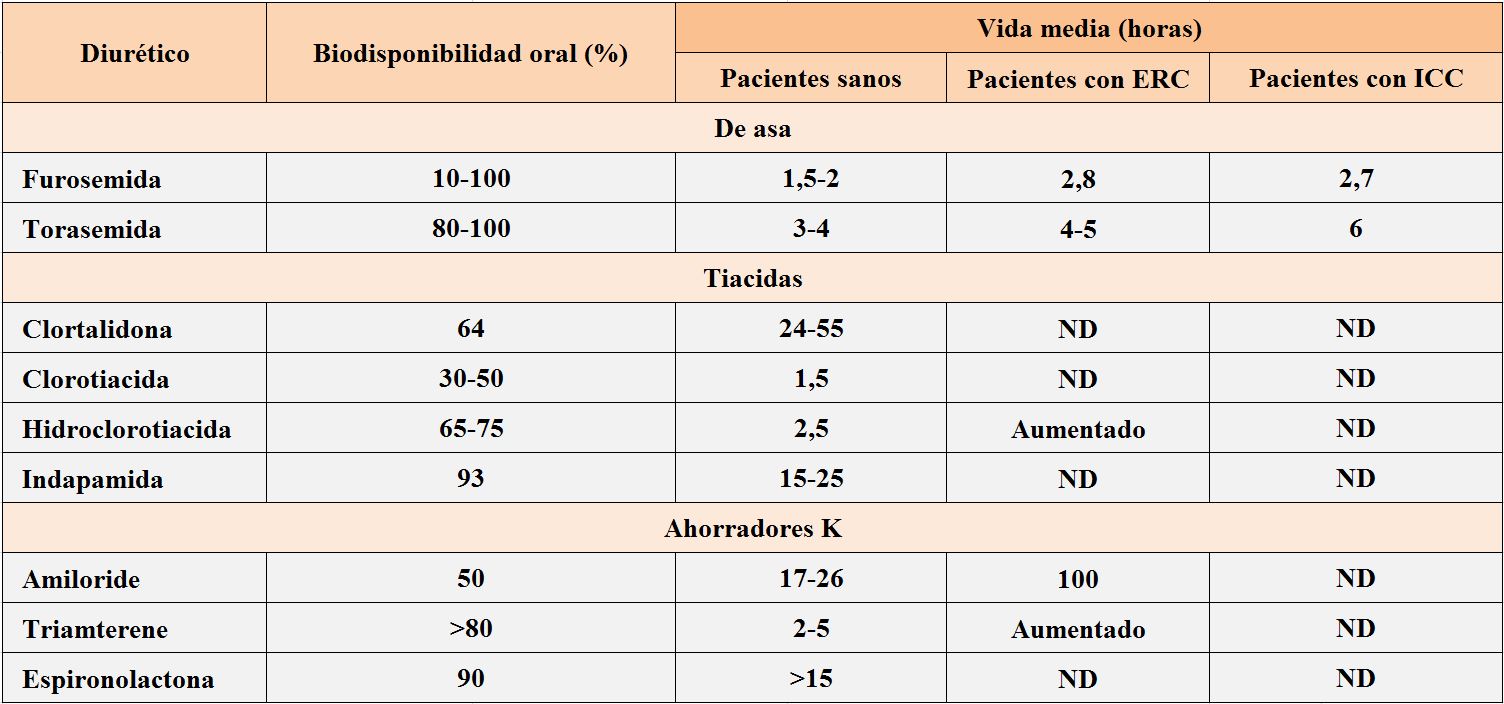
La furosemida, el diurético de asa más ampliamente utilizado, tiene una biodisponibilidad oral muy impredecible, oscila entre el 10-100% en condiciones fisiológicas. Este hecho explica la discordancia en la respuesta obtenida ante la misma dosis entre distintos pacientes, así como la diferente respuesta en un mismo paciente cuando la vía de administración es intravenosa u oral. El otro diurético de asa comercializado en España, la torasemida tiene una biodisponibilidad oral de 80-100%. Este dato justifica que algunos estudios hayan observado menor número de reingresos al alta domiciliaria después de un episodio de insuficiencia cardiaca en pacientes tratados con torasemida oral frente a los tratados con furosemida oral [1]. Como se observa en la (Tabla 1), las tiacidas tienen en general una biodisponibilidad oral bastante predecible, lo que justifica que no exista presentación parenteral para este grupo farmacológico.
La vida media de los diuréticos determina la frecuencia de su administración. Entre las tiacidas, hay dos de ellas con vida media suficiente para ser administradas solo una vez al día: indapamida (15-25 horas) y clortalidona (24-55 horas), mientras que otras como la hidroclorotiacida (2.5 horas) y la clorotiacida (1.5 horas) deberían ser administras dos o tres veces al día. La vida media de los diuréticos de asa varía entre las 2 horas de la furosemida, y las 4 horas de la torasemida. Esta vida media puede verse alargada en situaciones de ERC o insuficiencia hepática [2] [3]. Actualmente no disponemos de un diurético de asa de larga acción.
Farmacodinámica
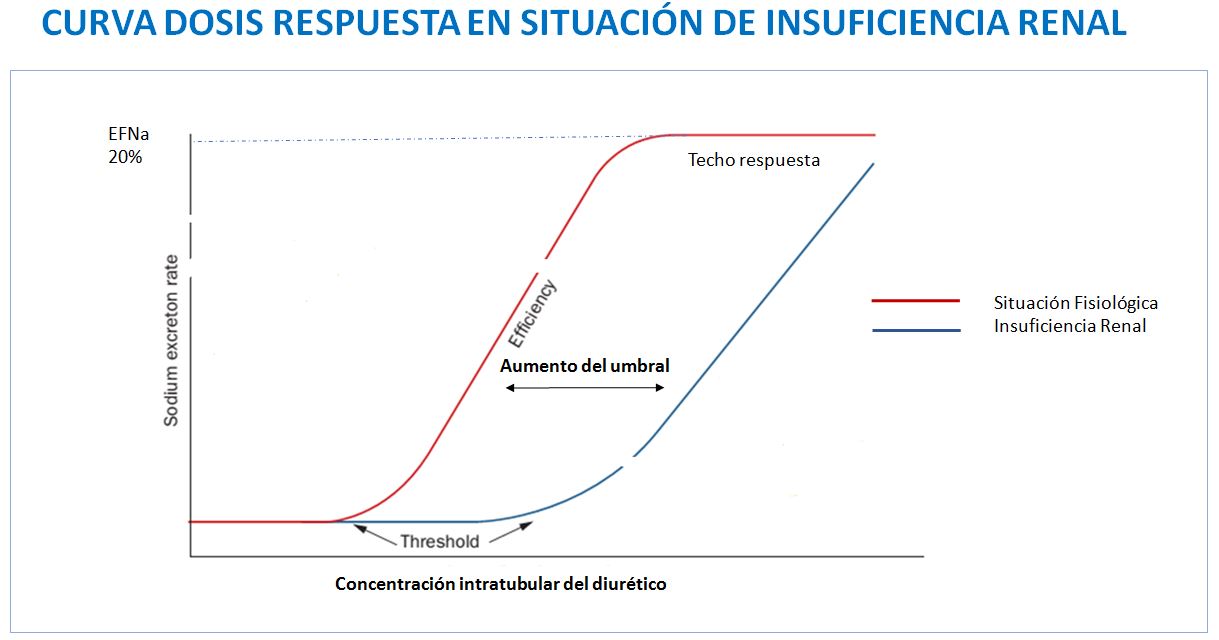
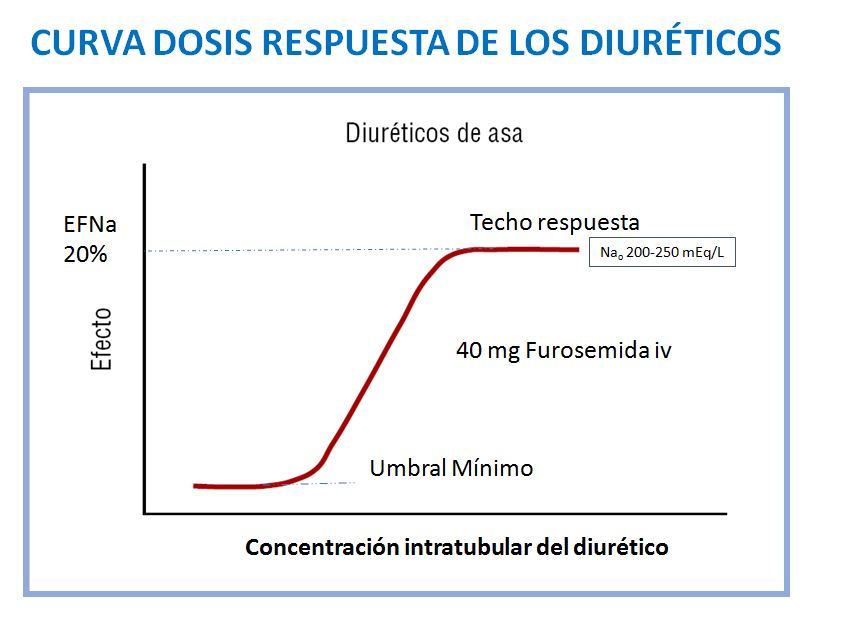
La relación entre la llegada de un diurético a su sitio de acción y su acción diurética-natriurética viene determinada por su farmacodinámica. La curva dosis respuesta de los diuréticos está dibujada en la (Figura 1). Esta curva es válida para todos los tipos de diuréticos.
Varias características farmacodinámicas de los diuréticos son clínicamente importantes. Existe un umbral mínimo en la concentración tubular del diurético necesario para obtener respuesta, y un umbral máximo a partir del cual no se va a conseguir un mayor efecto. La dosis efectiva debería estar entre el umbral mínimo y el umbral máximo. En situaciones fisiológicas, una dosis de 40 mg (2 ampollas) de furosemida es la dosis diurética-natriurética efectiva, y consigue la excreción de 200-250 mEq/l de sodio (20% del sodio filtrado) y de 3-4 litros de agua en un periodo de tres a cuatro horas. Teóricamente, una reducción en el filtrado glomerular y por tanto una reducción de la cantidad de agua y del sodio filtrado, podría limitar la respuesta máxima obtenida. Sin embargo, mecanismos compensadores existentes en situación de disminución del filtrado glomerular, como son un aumento de fluido procedente del túbulo contorneado proximal y una sobreexpresión de los transportadores tanto en el asa de Henle como en el túbulo distal, preservan, con alguna limitación, la respuesta diurética incluso en pacientes con descenso severo del FG. En esta situación se puede conseguir una respuesta diurética aceptable siempre que el diurético alcance el túbulo en concentración suficiente. Así, algunos estudios han mostrado que en pacientes con FG < 15 ml/min/1.73m2, la respuesta natriurética máxima (20% del Na filtrado) se puede alcanzar con una dosis de furosemida intravenosa de 160-200 mg o una dosis de torasemida oral de 80-100 mg. Algunas situaciones concomitantes como presencia de síndrome nefrótico o insuficiencia cardiaca puede limitar esta respuesta.
Tolerancia diurética
La eficacia de los diuréticos va disminuyendo con las dosis sucesivas, a este fenómeno se le ha llamado tolerancia. Se han descrito dos formas de tolerancia a los diuréticos, la tolerancia a corto plazo que se refiere a la respuesta compensatoria funcional renal en las horas siguientes a la administración de la primera dosis del diurético mediado por el sistema simpático y el sistema renina-angiotensina, y la tolerancia a largo plazo, que se refiere a una respuesta compensatoria morfológica, mediada por la hipertrofia de los segmentos distales de la nefrona. En ambos casos durante las horas siguientes a la desaparición del efecto del diurético, aparece un efecto antinatriurético tanto más intenso cuanto mayor ha sido la depleción de volumen inducida y mayor es la ingesta de sodio y agua, que finalmente llegan al túbulo, donde son ¿sobreabsorbidos¿. Este efecto puede contrarrestar completamente el efecto natriurético conseguido por el diurético, y anular el balance negativo, si dosis repetidas de diuréticos no son administradas.
Se han descrito varias estrategias para reducir el fenómeno de tolerancia a los diuréticos, entre ellas,
1. Restricción de la sal y líquidos en la dieta para prevenir la retención de sal post-diurética.
2. Administrar varias dosis diarias de furosemida, reduciendo el intervalo entre las dosis.
3. Añadir otra clase de diurético, sobre todo si son de larga vida media (eg. Clortalidona) que limite el efecto de la tolerancia a largo plazo entre la administración de las dosis.
4. Evitar suspender el diurético de forma abrupta.
5. Prevenir o revertir la alcalosis metabólica inducida por el diurético.
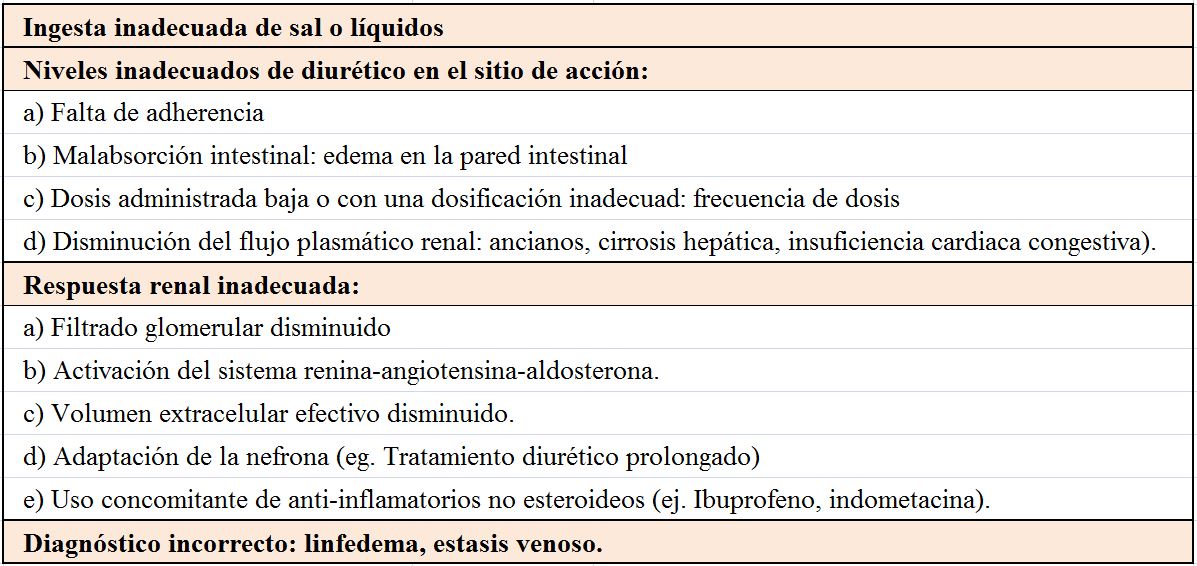
Resistencia diurética
La resistencia diurética define la situación en la que un paciente con sobrecarga hidrosalina no responde al tratamiento diurético. En la (Tabla 2), se han listado algunas de las situaciones clínicas que limitan la respuesta renal a los diuréticos e inducir resistencia a los mismos. Algunas de estas circunstancias realmente no suponen una verdadera resistencia a los diuréticos: la falta de adherencia a la restricción de agua y sal, la mala adherencia al tratamiento diurético, o incluso un diagnóstico incorrecto de sobrecarga de volumen como en el caso de linfedema o los edemas por fármacos dihidropiridínicos. Otras sí lo son, como el uso de concomitante de AINEs, no haber alcanzado la dosis mínima efectiva en situación de ERC, o haber empleado la furosemida por vía oral en lugar de por vía intravenosa, sobre todo en paciente con marcado edema en la pared abdominal o con mala biodisponibilidad individual. Su reconocimiento y corrección pueden transformar una situación de refractariedad a una situación de respuesta.
Finalmente hay otras situaciones clínicas muy evolucionadas en las que la optimización del tratamiento diurético no conlleva mejoría de la situación y suponen una verdadera resistencia a los diuréticos. Entre ellas la situación de ERC avanzada, la tolerancia a los diuréticos o la importante disminución del volumen circulante eficaz existente en situaciones tales como la insuficiencia cardiaca, la hipertensión portal o el síndrome nefrótico. Estas situaciones serán tratadas con más detenimiento en los próximos párrafos de este capítulo.
El uso de terapia combinada para bloquear secuencialmente más de un sitio en la nefrona, y así causar una interacción sinérgica entre diuréticos, puede ser una estrategia a considerar cuando la respuesta diurética no es la esperada. Así, la asociación de una tiacida puede potenciar considerablemente el efecto diurético de la furosemida. La asociación de la espironolactona no tiene un efecto diurético tan marcado, aunque puede contrarrestar el efecto hipokalemiante de la furosemida.
La acetazolamida es el único inhibidor de la anhidrasa carbónica con efecto diurético. Aunque actúa en el segmento proximal donde se absorbe la mayor parte del Na, su efecto diurético neto es mínimo por la múltiple compensación distal. Sin embargo, la acetazolamida puede corregir la alcalosis metabólica generada por el diurético de asa, y cuando se da junto a un diurético de asa y espironolactona/tiacida de forma secuencial su efecto diurético puede ser muy intenso.
Es importante destacar que tanto los diuréticos tiacídicos, los diuréticos proximales, como los inhibidores mineralcorticoides son exclusivamente de posología oral, y necesitan cierto tiempo para alcanzar el túbulo, a diferencia de los diuréticos de asa que cuando se administran parenteralmente llegan rápidamente. Por ello, para conseguir una verdadera sinergia, los diuréticos orales deben ser administrados varias horas antes, para que cuando los diuréticos de asa lleguen, estén activos.
Estrategia diurética en estados edematosos
El mecanismo de acción de los diuréticos en las situaciones clínicas de sobrecarga de volumen, como la insuficiencia cardíaca, la insuficiencia renal, el síndrome nefrótico o la hipertensión portal, no coincide con su mecanismo de acción en sanos. Conocerlo es fundamental para ofrecer el tratamiento deplectivo óptimo en cada situación.
Insuficiencia cardiaca
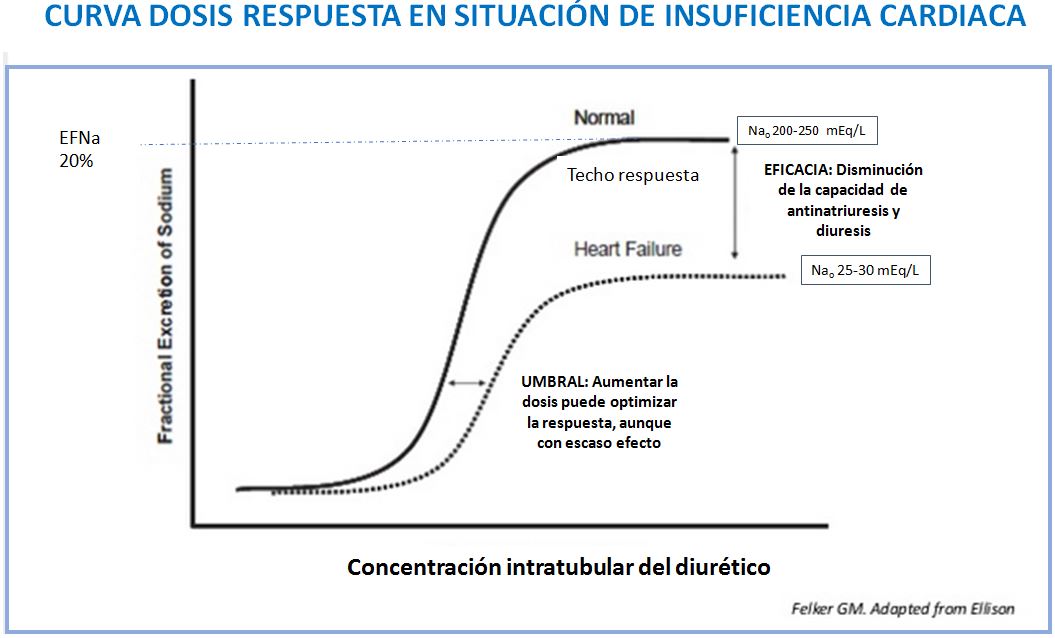
La respuesta a los diuréticos esta disminuida en situación de insuficiencia cardíaca. Se han identificado múltiples factores que justifican la mala respuesta al tratamiento diurético en pacientes con insuficiencia cardiaca, tales como el edema intestinal, que disminuye la absorción de los diuréticos orales, la hipotensión, la reducción del flujo sanguíneo renal y los cambios adaptativos en la nefrona que disminuyen la capacidad renal de natriuresis y diuresis.
En la (Figura 2), se puede observar como la curva dosis respuesta de los diuréticos en pacientes con insuficiencia cardiaca respecto a su efecto en condiciones fisiológicas, se desplaza discretamente hacia la derecha, pero sobretodo desciende su respuesta máxima. Por tanto, la primera estrategia en estos pacientes pasa por aumentar la frecuencia de administración del diurético. Aumentar la dosis en cada administración tiene un efecto limitado a menos que exista insuficiencia renal asociada. La utilización de la vía parenteral frente a la vía enteral puede ser útil en pacientes con baja biodisponibilidad o con edema intestinal [4].
El perfil farmacodinámico superior de la torasemida y su posible efecto vasorrelajador adicional probablemente explica la reducción de la mortalidad, la frecuencia/duración de la hospitalización relacionada con la insuficiencia cardíaca, o la clase funcional comparada con la furosemida, como se ha observado en algunos estudios [5].
Como se ha comentado, la sinergia de diuréticos en asa sobre todo con diuréticos tiacídicos ha demostrado ser eficaz en estados edematosos persistentes, y en concreto en aquellas situaciones de insuficiencia cardiaca con respuesta insuficiente al tratamiento diurético convencional [6].
En situaciones que implican una disminución importante del gasto cardiaco, el uso de inotropos o vasodilatadores, pueden ayudar a mejorar la situación cardiológica y forzar balance negativo con diuréticos.
Enfermedad renal crónica (ERC)
Los pacientes con insuficiencia renal se benefician de los diuréticos de asa, ya que conservan su utilidad, con limitaciones, hasta un filtrado glomerular (FG) inferior a 5 ml/min/1.73m2, mientras que los diuréticos distales teóricamente pierden su eficacia con FG 2. Sin embargo, los diuréticos tiacídicos mantienen sus efectos sinérgicos, incluso con FG bajos.
En situación de ERC, existe una disminución del número de nefronas, si bien las nefronas supervivientes mantienen su capacidad de respuesta a los diuréticos. El reto está en que el diurético llegue en concentración suficiente a la luz tubular para producir su efecto (Figura 3). En situación de ERC estadio 5, la máxima natriuresis ocurre con una dosis de 160-200 mg de furosemida IV o dosis equivalente de torasemida, y no se consiguen respuestas adicionales con dosis más amplias, aunque si es necesario, esta dosis se puede repetir varias veces al día.
Como se ha repetido en varias ocasiones, la respuesta diurética máxima es del 20% del Na filtrado, así en un paciente con un FG de 15 ml/min/1.73m2, la dosis máxima conseguirá una excreción de 75 mEq. Si la respuesta no es suficiente, dosis cada 4-6 horas pueden ser pautadas para que el balance final sea el deseado.
No podemos olvidar que en la ERC avanzada por retención de hidrogeniones aparece acidosis metabólica, que limita la llegada intratubular de los diuréticos de asa. La corrección de esta acidosis debe ser considerada para optimizar la respuesta a los diuréticos.
Síndrome nefrótico
La secreción tubular renal de los diuréticos no está limitada en el síndrome nefrótico. Si bien por su alta unión a proteínas, los diuréticos que finalmente alcanzan el túbulo se unen a las proteínas masivamente filtradas en situación de síndrome nefrótico, disminuyendo la cantidad de diurético, libre y por tanto activo. Sin embargo, algunos estudios sugieren que la unión a proteínas no afecta sustancialmente a la respuesta a furosemida [7].
Aumentar la dosis administrada podría aumentar la cantidad de diurético que llega al túbulo, saturar las proteínas que se eliminan, y por tanto aumentar la cantidad de diurético libre. Por tanto, ésta debería ser la estrategia fundamental para mejorar la respuesta diurética en caso pacientes con síndrome nefrótico. Si bien aumentar la frecuencia de la dosis y el uso concomitante de otros diuréticos también debe ser considerada.
La absorción de Na en pacientes con síndrome nefrótico está aumentada en los segmentos proximales, por la presencia de una angiotensina estimulada, y en los segmentos distales, mediado por la aldosterona. Por tanto la asociación de otros diuréticos ayuda a ampliar el efecto de los diuréticos de asa.
Hipertensión portal
Aunque el hiperaldosteronismo secundario está presente en todas las situaciones clínicas previamente descritas, este mecanismo compensatorio es más intenso en la hipertensión portal mediado por la vasoconstricción arterial renal. Por ello la familia diurética de elección en estos pacientes son los antialdosterónicos, que deberían mantenerse incluso cuando otros diuréticos sean añadidos.
Su capacidad diurética en general es muy discreta y para conseguir una respuesta diurética suficiente suele ser necesario asociar un diurético de asa desde el inicio. La hipertensión portal también es una situación desfavorable para la actuación de los diuréticos de asa: al igual que en la insuficiencia cardiaca en pacientes con cirrosis su respuesta máxima es muy limitada (natriuresis máxima 25-30 mEq de Na, comparado con 200-250 mEq en condiciones fisiológicas), y al igual que en situación de insuficiencia cardiaca aumentar la frecuencia de administración de los diuréticos de asa es la única alternativa posible. En caso de resistencia, por supuesto se podría añadir otros diuréticos.
En fases tempranas, la pérdida de peso diaria recomendada en estos pacientes es de hasta 0,5 kg y 1 kg, respectivamente, para prevenir la insuficiencia prerrenal [8]. En pacientes más evolucionados, con ascitis de gran volumen y malestar abdominal significativo, resistentes al tratamiento diurético, definida como uso de espironolactona 400 mg/día y furosemida 160 mg/día, se pueden beneficiar de una paracentesis terapéutica, en la que se pueden extraer 2-3 L de líquido ascítico diariamente (con correcta reposición con albúmina) sin que con ello reduzca considerablemente el volumen plasmático intravascular [9].
La espironolactona tiene una vida media corta, pero su vida media biológica es muy larga (2-4 días) por sus metabolitos. Es importante considerar esta característica para establecer su posología idónea (administración diaria o cada 48 horas), pero también para tratar posibles efectos secundarios severos como la hiperpotasemia.
Discontinuar el tratamiento con betabloqueantes, antagonistas de la angiotensina o los inhibidores de la enzima convertidora de angiotensina, puede mejorar la presión arterial, perfusión tisular, función renal y capacidad de respuesta diurética en pacientes con hipertensión portal.
Usos en otras indicaciones
Hipercalcemia / litiasis
Los diuréticos osmóticos y de asa aumentan la excreción urinaria de Ca2+, mientras que las tiacidas y los diuréticos distales la disminuyen. La hipercalcemia activa el receptor sensible a calcio (RSCa) en la glándula paratiroides, que inhibe la reabsorción de agua y NaCl en el asa ascendente de Henle y altera la concentración renal. La depleción en el volumen extracelular consecuente limita la excreción de Ca2+ al reducir el filtrado glomerular y aumenta la reabsorción de agua y Ca2+ a nivel proximal. Por lo tanto, la terapia inicial de la hipercalcemia debe incluir siempre la expansión del volumen con salino, y bisfosfonatos, dependiendo de la causa. Los diuréticos de asa pueden prevenir o tratar la sobrecarga de volumen, pero existe poca evidencia que apoye su uso indiscriminado en el tratamiento de la hipercalcemia [10].
Las tiacidas disminuyen el riesgo de formación de litiasis en paciente con hipercalciuria o hiperoxaluria, al reducir la excreción de Ca2+ y oxalato [11]. La disminución de la calciuria se puede reforzar con amiloride [12] y una dieta baja en sal.
Diabetes Insípida
Las tiacidas pueden reducir hasta un 50% del volumen diurético en pacientes con diabetes insípida central o nefrogénica [13]. Este efecto paradójico está en relación con la disminución del filtrado glomerular, el aumento de la reabsorción de agua en la nefrona proximal y distal [14] y un aumento en la osmolaridad medular que conlleva a la reabsorción de agua a nivel distal. Un pequeño ensayo clínico cruzado y controlado con placebo, demostró que el amiloride previene la poliuria inducida por litio [15]. Este efecto se atribuye al bloqueo mediado por amiloride de la entrada de litio por ENaC en la célula principal, donde puede infrarregular los canales de acuaporina 2, via glucógeno sintasa quinasa 3.
HTA
Los diuréticos son útiles en el manejo de la HTA en pacientes con insuficiencia renal crónica y sin ella. De forma general, los diuréticos tiacídicos están recomendados en pacientes con ERC estadio 1-3 y los diuréticos de asa en los estadios 4-5.
Acidosis tubular renal
La furosemida aumenta el transporte distal de NaCl y estimula la secreción de aldosterona y aumenta la fosfaturia, con lo que favorece la eliminación de ácidos [16]. Además, existe un efecto directo de la furosemida y las tiacidas sobre la acidificación distal al aumentar la subunidad B1 de H+-ATPasa [17]. Por lo tanto, la furosemida puede ser utilizada en la acidosis renal tubular tipo IV para aumentar la excreción renal de ácido [18].
Osteoporosis
Las células óseas contienen un cotransportador Na+- Cl- que cuando es inhibido por una tiacida, aumentan la captación ósea de calcio [19]. Las tiacidas inhiben la osteocalcina, una proteína específica de los osteoblastos que retrasa la formación de hueso, y directamente estimula la producción de los marcadores de diferenciación osteoblástica; osteopontina y runx2 [20].
Las tiacidas inhiben la reabsorción ósea y aumentan la mineralización ósea, independientemente de la hormona paratiroidea [21]. Por lo tanto, las tiacidas promueven la mineralización ósea tanto por reducción de la excreción renal de calcio y por efectos directos sobre los huesos. En varios ensayos clínicos, las tiacidas se han asociado con un aumento en la densidad mineral ósea y una disminución de las fracturas de cadera en ancianos [21]
Síndrome de Gitelman
Además de la suplementación oral de potasio, los diuréticos ahorradores de potasio se pueden utilizar en el Síndrome de Gitelman. La espironolactona (200-300 mg/día) demostró ser superior al amiloride (30 mg/día) y eplerenona (150 mg/día) en corregir la hipokaliemia en un ensayo clínico.
Efectos secundarios de los diuréticos
Alteraciones hidroelectrolíticas
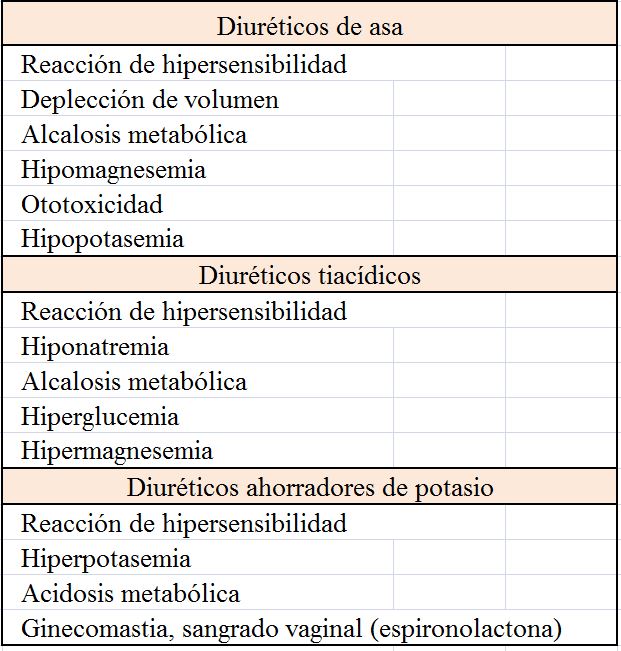
La lista de efectos secundarios de los diuréticos es extensa. La mayoría de ellos están relacionados con su efecto diurético, aunque hay otros específicos de los fármacos, como las reacciones idiosincráticas.
Las alteraciones hidroelectrolíticas son los efectos secundarios más comunes y éstas están relación con la duración del efecto más que con la intensidad del mismo. Así por ejemplo los diuréticos tiacídicos, tales como la clortalidona, aunque menos potente que los diuréticos de asa producen una hipopotasemia e hipomagnesemia más intensa, por su mayor vida media. Las alteraciones hidroelectrolíticas más frecuentes asociadas al uso de diuréticos son: hiponatremia, hipo/hiperkaliemia, hiperuricemia, hiper/hipocalcemia
Hiponatremia
Es un efecto secundario poco frecuente pero con importantes complicaciones potenciales asociadas, sobre todo en pacientes con ERC, en los que este efecto secundario aparece con más frecuencia. Su aparición es más frecuente con el uso de diuréticos tiacídicos que con diuréticos de asa y suele aparecer en las primeras semanas tras el uso del diurético, aunque a veces aparece varios años después.
La restricción de agua y la eliminación del diurético suele ser suficiente para corregirlo. Si el uso del diurético es necesario, el uso de otra familia de diurético puede evitar su reaparición.
Hipo/Hiperkaliemia
La hipopotasemia es inducida por los diuréticos de asa y tiacídicos, clásicamente llamados diuréticos perdedores de potasio y la hiperpotasemia por los diuréticos distales, clásicamente llamados, diuréticos ahorradores de potasio (espironolactona, eplerenona, amiloride y triamterene).
El mecanismo fundamental que induce la hipopotasemia tras el uso de diuréticos, es el incremento del flujo distal, que está aún más aumentado en situación de alta ingesta de sodio. Por ello, el tratamiento efectivo de la hipopotasemia inducida por diuréticos, además de retirar/disminuir la dosis de diurético, añadir suplementos de potasio o incluso la utilización de diuréticos ahorradores de potasio, deben incluir la restricción de Na.
En el caso de los diuréticos ahorradores de potasio, el mecanismo que produce hiperpotasemia es inherente a su mecanismo de acción, el Amiloride y triamterene bloqueando los canales epiteliales de Na, y por tanto evitando la eliminación de hidrogeniones/potasio, la espironolactona y eplerenona compitiendo con el receptor mineralcorticoide. Esta complicación es más probable en situación de ERC, sobre todo en pacientes ancianos o diabéticos, en pacientes que concomitantemente reciben fármacos de la familia de los IECA, ARA2 o AINES, o en aquellas situaciones predisponentes a hiperpotasemia, como la acidosis, administración de trimetoprim-sulfametoxazol o heparina.
Hiperuricemia
De forma general cualquier diurético puede producir hiperuricemia por aumento de su reabsorción tubular proximal inducida por la reducción del volumen circulante eficaz. Este efecto puede incrementarse en el caso de los diuréticos tiacídicos o de asa, puesto que compiten por los mismos transportadores de aniones orgánicos.
Hiper /Hipocalcemia
Previamente ya se ha comentado que los diuréticos tiacídicos disminuyen la excreción de calcio en la orina y que los diuréticos de asa lo aumentan. Por estos mecanismos, la furosemida puede favorecer en pacientes con ERC, sobre todo si es avanzada, el desarrollo de hiperparatiroidismo secundario y por el contrario el tratamiento con tiacidas puede producir hipercalcemia en paciente con hiperparatiroidismo primario asintomático hasta ese momento.
Reacciones idiosincráticas
Lesiones cutáneas por sensibilidad han sido descritas para todos los diuréticos, aunque con mayor frecuencia para los diuréticos tiacídicos. Posiblemente este efecto está relacionado con la sensibilidad cruzada que todos ellos tienen con las sulfamidas. Otros efectos secundarios severos son, la pancreatitis necrótica o la nefritis tubulointersticial aguda.
Se han descrito casos de ototoxicidad con los diuréticos de asa, sobre todo cuando estos son administrados rápidamente, alcanzando concentraciones pico muy elevadas. En un metanálisis del uso de furosemida en pacientes con AKI, la odds ratio para el desarrollo de sordera fue mayor de 3 cuando la dosis de furosemida excedía 1-3 g/día [4]. En la mayoría de los casos la ototoxicidad es reversible, aunque se han descrito casos que no lo han sido.
En resumen, los diuréticos son unos fármacos de amplísimo uso en la práctica clínica diaria. A pesar de ello, sus características farmacodinámicas y farmacocinéticas distan mucho de ser las ideales sobre todo cuando se usan en condiciones de sobrecarga de volumen extracelular. En espera de que aparezcan nuevas moléculas, solo el conocimiento de sus limitaciones y de las estrategias necesarias para superarlas nos ayudaran a conseguir la respuesta diurética que el paciente necesita.