Manejo de la hipertensión arterial y la proteinuria asociada al tratamiento oncológico: Anti VEGF e Inhibidores de la Tirosina Quinasa
1. Introducción
La vía del factor de crecimiento endotelial vascular (Vascular Endothelial Growth Factor,VEGF) es una diana terapéutica fundamental en oncología, ya que el VEGF es un factor clave en la angiogénesis y la progresión tumoral, así como en la metástasis. Desde el desarrollo de Bevacizumab, el primer anticuerpo recombinante contra VEGF, posteriormente se han ido comercializando más agentes que actúan sobre la vía VEGF o sus vías downstream. Según su mecanismo de acción concreto, estos agentes tienen un perfil característico de efectos adversos a pesar de actuar todos en la vía “VEGF”, como se irá detallando más adelante[1].
Los fármacos que inhiben esta vía (Inhibidores del VEGF o VEGFi) se utilizan ampliamente en tumores sólidos como el carcinoma de células renales (RCC) o el carcinoma hepatocelular (HCC). A pesar de sus beneficios, esta inhibición provoca ciertos efectos colaterales, manifestados principalmente como hipertensión, proteinuria y microangiopatía trombótica (MAT), mayoritariamente limitada al riñón [2].
A día de hoy, ante la ausencia de evidencia sólida, no se ha establecido ninguna estrategia definitiva universalmente aceptada para el manejo de los efectos adversos a nivel renal de estos agentes, especialmente la proteinuria. Así que las recomendaciones existentes son básicamente en base a resultados de estudios observacionales y a consenso de expertos.
Agentes anti-VEGF (directos) vs inhibidores tirosina quinasa (TKI)
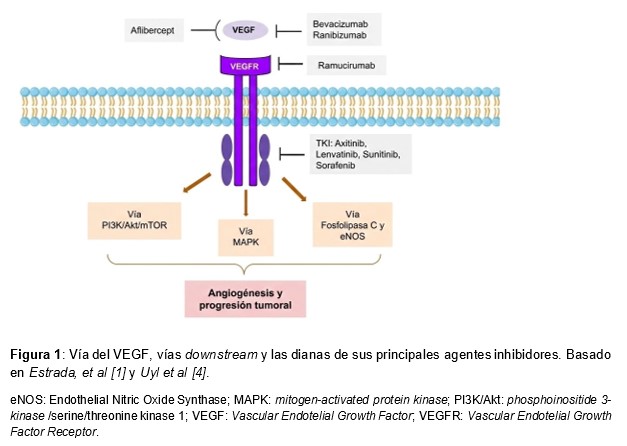
Los VEGFi pueden clasificarse según su diana en la vía VEGF, ya sea directamente a nivel de VEGF o de su receptor VEGFR (Vascular Endothelial Growth Factor Receptor). Los distintos mecanismos de acción serían: fármacos que se unen directamente a VEGF, los que “secuestran” VEGF, los que inhiben el receptor VEGF o bien inhiben las tirosinas quinasas de estos receptores o sus vías posteriores (más downstream), como se muestra en la (Figura 1). Los agentes “anti-VEGF” específicamente, incluyen el bevacizumab y ranibizumab (acción anti VEGF directa), aflibercept (acción de "trampa" VEGF) y ramucirumab (acción inhibitoria del VEGFR). Los inhibidores de tirosina quinasa (TKIs) de la vía del VEGF, por otro lado, actúan no solo en el receptor de tirosina quinasa (RTKs) de la vía VEGF, sino en otras familias de RTKs, como el PDGFR (Platelet Derived Growth Factor Receptor), el FGFR (Fibroblast Growth Factor Receptor) o el EGFR (Epidermal Growth Factor Receptor). Por eso muchas veces se les conoce como "multitargeted TKIs", y tienen un perfil de efectos adversos variado y que depende de su grado de especificidad. Los principales agentes que actúan sobre la vía del VEGFR (pero también en otras vías) son: sunitinib, pazopanib, sorafenib, axitinib y lenvatinib, entre muchos otros [1]. A pesar de ser “multitargeted”, cabe destacar que, en general, cuanta más afinidad para la inhibición selectiva de la vía VEGF, más incidencia de efectos adversos cardiovasculares y renales, siendo el bevacizumab el más paradigmático [3].
2. Epidemiología según el Agente Utilizado
En referencia a la hipertensión, los VEGFi presentan una incidencia global que oscila entre el 30 y el 80% según las series [5,6]. Si lo desglosamos por agentes, la incidencia de hipertensión en pacientes tratados con bevacizumab es alrededor del 23-34%, con un metaanálisis que mostraba que el 8,2% de todos los pacientes mostraron hipertensión grave (definida como TA >160/100 mmHg), con un riesgo relativo para desarrollarla de 5,2 (IC 95% 4,188-6,390), siendo este riesgo dosis-dependiente [3]. Según un metaanálisis de estudios japoneses, los agentes que más se relacionan con la aparición de hipertensión serían sunitinib (51%) o axitinib (75%), un agente anti-tirosina-quinasa del receptor de VEGF [7]. En una revisión reciente, los agentes que más se relacionan con HTA serían: ponatinib (53-74%), axitinib (50%) y lenvatinib (47%), mientras que el sunitinib reportan una incidencia menor (22-41%) [4].
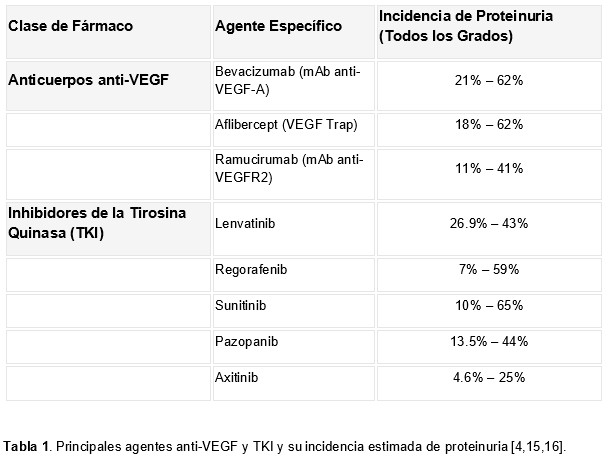
La proteinuria, también es un evento adverso común y dosis-dependiente, y se considera un marcador directo de nefrotoxicidad. Su incidencia puede variar ampliamente dependiendo del fármaco, la dosis y las características del paciente (enfermedad renal crónica de base, comorbilidades, etc.). La tasa global de incidencia de proteinuria (todos los grados) de los distintos agentes anti-VEGF (Bevacizumab, Ramucirumab y Aflibercept) es de aproximadamente el 25-60% según las series, con una incidencia del 3% para los grados severos (Grado ≥ 3). La incidencia de proteinuria grave (grado 3 o 4) con Bevacizumab específicamente, oscila entre el 2 y el 32%, y la de síndrome nefrótico de menos del 0,1% [8]. Con los TKI la incidencia oscila entre el 6 y el 34% según agente, y entre el 1 y el 10% para proteinuria grado 3 o superior. El Lenvatinib en concreto suele mostrar una incidencia en el extremo superior del rango [9]. En la (Tabla 1) se muestran los principales agentes y su incidencia de proteinuria.
Si nos centramos en las lesiones histopatológicas a nivel renal, la más frecuentemente descrita con el uso de anti-VEGF es la MAT [6,10], siendo la incidencia variable según las series, pero en una de las más importantes (Izzedine H, et al [6]), la incidencia era del 73% de los casos biopsiados (de un total de 100 biopsias), siendo la presentación clínica más frecuente la proteinuria en rango subnefrótico. Otra serie más reciente, de la Mayo Clinic, reporta una incidencia similar, pero incluyendo solo 19 casos [11]. Aproximadamente el 50% de los casos de MAT relacionada con VEGFi, son limitados al riñón, como se ve en la misma cohorte citada anteriormente (Izzedine H, et al [6]) y como también se hace referencia de forma indirecta en un amplio estudio francés más reciente, que incluía 757 casos de MAT renal [12]. Asimismo, también hay casos descritos, con mucha menor frecuencia, de podocitopatías (cambios mínimos -MCD- y variante colapsante de la GEFS), GN crioglobulinémica o glomerulonefritis crescéntica pauciinmune [6,13,14].
3. Fisiopatología e histopatología
El VEGF se expresa en varios tipos de células del organismo, incluyendo células endoteliales, macrófagos, podocitos, entre otras. A parte de su papel conocido en la angiogénesis, la vía VEGF también es esencial en la regulación del tono vascular, así como lo es en el mantenimiento de la barrera de filtración glomerular [4]. Seguidamente se detallarán los mecanismos que inducen la hipertensión y proteinuria con los VEGFi.
Hipertensión
Con respecto a la fisiopatología de la hipertensión en relación con los VEGFi, se han propuesto distintos mecanismos. Estos mecanismos, a modo resumido, afectan al desarrollo de hipertensión de distintos modos: el aumento de la resistencia vascular periférica, el aumento del estrés oxidativo, la reducción de la linfangiogénesis, así como el aumento de la retención de agua y sodio a nivel renal [17]. Por lo que hace a la resistencia vascular periférica, la vía de VEGF regula el tono vascular mediante el aumento de la liberación de factores paracrinos vasodilatadores como el óxido nítrico (NO) y prostaciclinas (PGI2), mientras que disminuiría la producción de factores vasoconstrictores como la endotelina (ET)-1. Así, con los VEGFi, ocurre un disbalance entre los factores vasoconstrictores y vasodilatadores que es lo que conduce a la HTA [18][19]. En referencia a la retención salina a nivel renal, se produce por dos mecanismos principales, en primer lugar, la vía del propio NO, la cual interviene en el proceso de feedback tubuloglomerular y la natriuresis por presión [20]. En segundo lugar, mediante la vía de las prostaglandinas, la inhibición de la cual provoca disminución de la perfusión glomerular y mayor retención de sodio y agua [21].
Proteinuria
La proteinuria inducida por los VEGFi se debe principalmente a la interrupción del equilibrio que mantiene la barrera de filtración glomerular. En el riñón, el VEGF se expresa tanto a nivel de los podocitos como de las células tubulares epiteliales. Por otro lado, el receptor de VEGF se expresa en el endotelio capilar tanto del glomérulo como de los capilares peritubulares. Esto permite, en condiciones fisiológicas, una correcta adecuación de la perfusión glomerular y mantenimiento de la barrera de filtración glomerular [22]. En modelos murinos, se ha visto que tanto la sobreexpresión de VEGF como su ausencia conlleva la aparición de diversas glomerulopatías, básicamente representadas por daño endotelial (endoteliosis, MAT) y podocitopatías (glomeruloesclerosis focal y segmentaria, glomerulopatía colapsante) [23][24]. Por último, la exposición crónica a los VEGFi, se ha visto que acaba distorsionando la red capilar peritubular, conduciendo a hipoxia renal y finalmente evolucionando a fibrosis e insuficiencia renal progresiva [25].
Histopatología renal con relación a los VEGFi
En general, las biopsias de pacientes tratados con anti-VEGF suelen mostrar más frecuentemente hallazgos compatibles con MAT que los TKIs [26]. Mientras que estos segundos, suelen asociarse más con podocitopatías [6]. Estas diferencias se estima que son debidas a la sobreexpresión de ciertos mediadores en mayor o menor medida en función de si la inhibición es más proximal o distal en la vía. Así, con los anti-VEGF el VEGFA se ve aumentado y esto hace que aumente la expresión de la vía NF-kB y la translocación de RelA a nivel de la célula endotelial, lo cual acaba estimulando la activación del complemento por una “downregulation” del factor H [27]. Por su parte, la inhibición a nivel de la tirosina quinasa del VEGFR, activa otras vías (mediada básicamente por la sobreexpresión de c-mip al podocito) que acaban llevando a alteraciones del citoesqueleto mediante la inhibición de la fosforilación de la nefrina. Los efectos sobre el complemento por parte de los TKIs no están bien dilucidados [28][29].
Así, en general, la inhibición del VEGF puede provocar dos categorías principales de lesiones glomerulares que podemos observar [15]:
1. Microangiopatía Trombótica (MAT).
Esta lesión, como se ha comentado, es más frecuente con los anticuerpos anti-VEGF (como el Bevacizumab) que con las VEGF traps (como Aflibercept) o los TKI. La MAT se caracteriza por lesión y disfunción de la célula endotelial glomerular. A diferencia de otros tratamientos oncológicos que suelen producir MAT sistémica (como la gemcitabina), los VEGFi suelen producir MAT limitada al riñón [30]. Esta disfunción conduce a MAT limitada al riñón, que se manifiesta histológicamente como:
a. Pérdida de fenestraciones endoteliales debido al edema celular (endoteliosis)
b. Mesangiolisis
c. Aparición de microtrombos de fibrina a nivel de capilares glomerulares.
d. Aparición de dobles contornos en la membrana basal glomerular (MBG)
e. La lesión endotelial también se ha relacionado con la reducción a nivel local del Factor H (CFH), aumentando la vulnerabilidad a la activación del complemento y al daño microvascular [32].
2. Podocitopatías (MCD/GEFS):
Esta lesión es más propia de los Inhibidores de la Tirosina Cinasa (TKI) (Sunitinib, Sorafenib, Pazopanib, Axitinib).
a. Pérdida de fenestraciones endoteliales
b. En ocasiones también se observa proliferación de las células endoteliales
c. Borramiento de los pedicelos podocitarios (foot process effacement), que puede conllevar a pérdida del propio podocito, observados en la microscopía electrónica.
3. Lesiones Adicionales:
Otras lesiones descritas en relación con los VEGFi, menos frecuentes, son: nefritis tubulointersticial aguda (NTIA), necrosis tubular aguda (NTA) o, aún menos frecuentemente, otras glomerulopatías (como glomerulonefritis mediada por immunocomplejos, glomerulonefritis proliferativa extracapilar o nefropatía IgA) [2][32].
4. Manejo de la Hipertensión Inducida por VEGFi
La hipertensión arterial (HTA) en los pacientes tratados con VEGFi es un efecto adverso dosis-dependiente, que además refleja una adecuada inhibición de la vía VEGF. Muchos autores sugieren que la aparición de HTA durante el tratamiento se traduce en mejor pronóstico a nivel neoplásico, pero un metaanálisis de varios ensayos clínicos demostró que no había un claro valor predictivo positivo en relación con la aparición de hipertensión [33]. Si bien es verdad que hay descritos algunos casos concretos de neoplasia donde sí que podría haber una relación entre la HTA y un mejor pronóstico del cáncer, como por ejemplo en cáncer gástrico [34].
En pacientes con HTA crónica, previa al inicio del tratamiento, hay que asegurar un buen control tensional antes del inicio de los VEGFi [35]. Dado que la hipertensión con relación a los VEGFi suele aparecer a los pocos días de recibir el tratamiento, se recomienda control de la presión arterial semanalmente a nivel hospitalario o a diario mediante la automedida de la presión arterial ambulatoria (AMPA).
En muchos casos, como se ha comentado, la HTA es dosis dependiente, con lo que al disminuir la dosis o retirar el tratamiento, se suelen normalizar las cifras de presión arterial (PA). Pero en el contexto de pacientes con neoplasias avanzadas que requieren de dichos tratamientos, hay que intentar mantenerlos, a menos que haya cifras tensionales excesivas (PA > 180/120 mmHg) o complicaciones serias derivadas de la HTA: síndrome de encefalopatía posterior reversible–en inglés PRES-, ictus hemorrágico, infarto agudo de miocardio, etc. En dichos casos, habría que suspender el tratamiento y proceder al tratamiento de la emergencia HTA [36].
El dintel de presión arterial para iniciar tratamiento antihipertensivo en estos pacientes no difiere mucho de los habituales con los que trabajamos en práctica clínica, aunque se debería de individualizar. En pacientes sin factores de riesgo cardiovascular clásicos ni comorbilidades como diabetes, enfermedad aterosclerótica o insuficiencia renal crónica, se puede considerar ser más permisivo y empezar a tratar si la PA excede los 140/90 mmHg. Mientras que, en pacientes con alguna de estas comorbilidades, al sobrepasar los 130/80 mmHg, se debería considerar ya el inicio de tratamiento [37]. Al contrario, en pacientes con cierta fragilidad y/o enfermedad cancerosa metastásica avanzada y expectativa vital corta, los objetivos de PA deben ser más laxos, con tal de minimizar la mala tolerancia al tratamiento antihipertensivo [38].
Los agentes de primera elección en la HTA mediada por VEGFi son los IECA/ARA-II. Esto es así por su efecto antagónico con respecto a la inhibición de la vía VEGF, así, se consigue aumentar de nuevo el NO de la microcirculación, así como contrarrestar la retención hidrosalina mediante la inhibición de la acción de la angiotensina II [39]. Además de su efecto antihipertensivo por estas vías, poseen el ya conocido efecto antiproteinurico deseado en estos pacientes, por lo que son el tratamiento de elección. Como dato añadido, cabe señalar que algunos reportes sugieren que los IECA/ARA-II podrían tener además un efecto sinérgico antitumoral con los VEGFi y aumento de la supervivencia global, sobretodo descrito en cáncer renal [40]. Si no se consigue un buen control tensional, se considerarán agentes de segunda línea los calcioantagonistas dihidropiridínicos (amlodipino, nifedipino, etc.). Hay que evitar el uso de calcioantagonistas no dihidropiridínicos (verapamil, diltiazem) en pacientes tratados con TKI, puesto que interfieren en su metabolismo mediante inhibición del citocromo P450, aumentando su vida media y empeorando entonces la hipertensión [36]. Otros agentes que se pueden considerar son los b-bloqueantes no selectivos (carvedilol o nebivolol), que incluso podrían conferir un efecto aditivo antiangiogénico [41]. También se pueden usar diuréticos, aunque en general habría que usarlos con prudencia en los pacientes con neoplasias avanzadas en régimen de quimioterapia por el riesgo inherente que tienen a la depleción de volumen por múltiples causas: inapetencia, vómitos, diarrea, etc. que conllevan al deterioro de la función renal. Por último, otros agentes vasodilatadores como doxazosina, hidralazina o incluso nitroglicerina, se pueden considerar, pero llegado a este punto probablemente habría que plantear un ajuste de dosis del VEGFi, puesto que estaríamos con una HTA de difícil control.
El rol de los antagonistas de la endotelina en estos pacientes no está bien demostrado. Si bien es verdad que tiene un sentido fisiopatológico (al estar sobreexpresada la endotelina-1) y en modelos animales hay resultados prometedores, en humanos su uso no está aprobado por agencias del medicamento. Además, hay que tener en cuenta que tienen el riesgo de favorecer la aparición de edema [42].
En relación con los iSGLT-2, se ha visto que aparte de sus beneficios cardiovasculares y de poseer un leve efecto antihipertensivo, también poseen un efecto protector de la célula endotelial. Asimismo, los iSGLT2 tienen un efecto modulador sobre la ET-1, disminuyendo de forma discreta sus niveles, por lo que podrían ser beneficiosos en los pacientes tratados con VEGFi. Sin embargo, su papel para mitigar la toxicidad vascular inducida por anti-VEGF aún requiere confirmación clínica [43][44].
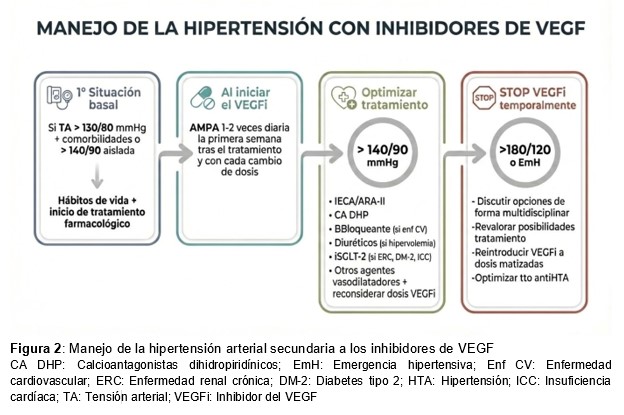
Por lo que hace a hábitos de vida, sirven los mismos consejos prácticamente que en población general. En lo que a la dieta se refiere, una dieta hiposódica es igualmente recomendable. Esto se observó en un ensayo clínico “SUN-SALT study”, donde se vio que la restricción de sodio (< 4 g de sal al día) era eficaz para reducir la elevación de la PA en pacientes tratados con VEGFi, así como la aparición de proteinuria [45]. Otras medidas como mantener un peso adecuado, fomentar el ejercicio físico, disminuir consumo de alcohol o cafeína, así como controlar el dolor o la ansiedad, son igualmente importantes en este subgrupo de pacientes [46]. En la (Figura 2) se muestra un esquema orientativo de cómo manejar la HTA inducida por VEGFi.
5. Manejo de la Proteinuria Inducida por VEGFi
La proteinuria en relación con los VEGFi, en la mayoría de los pacientes, es de baja cuantía y no suele presentarse como síndrome nefrótico. Si bien es verdad que la proteinuria habitualmente se relaciona con la progresión a insuficiencia renal terminal (IRCt), un metaanálisis de 47 ensayos clínicos con bevacizumab, ramucirumab y aflibercept, vio que el uso de estos agentes no aumentaba de forma estadísticamente significativa el riesgo de IRCt. Probablemente esto nos indica que, en los casos más graves, el hecho de suspender el fármaco conlleva a una reducción de la proteinuria y por tanto también del riesgo de progresión a IRCt [47].
La proteinuria se suele clasificar según su cantidad/gravedad siguiendo los siguientes criterios:
· Proteinuria Leve a Moderada: La forma más común, proteinuria generalmente < 2g, y lo más frecuente es que esté alrededor de 0,5-1g.
· Proteinuria Grave: En el contexto del tratamiento con VEGFi, se considera proteinuria grave cuando sobrepasa los 2g, por sus implicaciones en el manejo.
· Síndrome Nefrótico: La forma más infrecuente y grave.
· Otros hallazgos concomitantes: La proteinuria puede ir acompañada de Daño Renal Agudo (AKI), especialmente en casos de MAT, donde se puede observar además hematuria microscópica.
Proteinuria relacionada con la propia neoplasia
A tener en cuenta en el diagnóstico diferencial, si la proteinuria puede esconder una glomerulopatía secundaria a la propia neoplasia, más que ser un efecto adverso de los fármacos. En estos casos es clave el curso evolutivo de la proteinuria y disponer de estudios basales antes de iniciar los tratamientos. Las glomerulopatías más asociadas, en el caso de tumores sólidos de estirpe epitelial, son la nefropatía membranosa o la glomerulonefritis membranoproliferativa mediada por inmunocomplejos. Una revisión sistemática de hace unos años, analizó la incidencia de procesos malignos en pacientes con nefropatía membranosa, siendo esta aproximadamente del 10% (95% CI 6,1-14,6) [48].
El manejo en estos casos requiere una evaluación de riesgo-beneficio en colaboración multidisciplinaria.
A. Evaluación y Monitorización
1. Evaluación Basal: La proteinuria debe cuantificarse antes de iniciar la terapia, preferiblemente mediante el cociente proteína/creatinina en orina (UPCR) junto al cociente albúmina/creatinina en orina (UACR), siendo el análisis de orina con tira reactiva menos indicado. Si hay proteinuria significativa (> 2g/g), se recomienda investigar la causa y tratarla antes de iniciar el VEGF siempre que sea posible, balanceando el riesgo de retrasar el inicio del tratamiento oncológico.
2. Monitorización Regular: Se recomienda monitorizar la PA y realizar análisis de orina antes de cada ciclo de tratamiento.
3. Papel de la biopsia renal: A pesar de ser el gold-standard para filiar la etiología de la proteinuria en los pacientes tratados con VEGFi, la realidad es que en práctica clínica habitual no se realiza de forma rutinaria la biopsia renal. Esto se debe a varios factores: efecto adverso conocido, mejoría de la proteinuria al disminuir la dosis del fármaco, pacientes nefrectomizados y la asunción de que muchas veces la biopsia no cambiará el manejo. Pero debería considerarse su realización sobretodo en los casos de proteinuria nefrótica o insuficiencia renal aguda con o sin microhematuria de novo confirmada, sobretodo buscando descartar lesiones de MAT en la biopsia o descartar que la proteinuria no sea directamente un evento paraneoplásico, lo cual cambiaría el manejo radicalmente: implicaría “intensificar” tratamiento oncológico en vez de suspenderlo [49][50].
B. Intervenciones Farmacológicas
No existe evidencia sólida para establecer un esquema de manejo categórico, pero las distintas sociedades científicas suelen coincidir en esquemas similares al siguiente:
· Proteinuria de Grado Bajo (< 2 g): El tratamiento puede continuar en la mayoría de los casos.
o Primera Línea: Como comentábamos en el apartado de hipertensión, los inhibidores del sistema renina-angiotensina (IECA/ARA-II), se consideran el tratamiento de primera línea para reducir la proteinuria y tratar la hipertensión asociada debido a sus efectos renoprotectores y antiproteinúricos. Hay algún estudio preclínico que sugiere que los IECA podrían tener un efecto deletéreo a nivel de la progresión tumoral, sobretodo en hepatocarcinoma, mediante su mecanismo de aumento de la síntesis de EPO renal, y esto podría conllevar resistencia a los VEGFi [51]. Pero estos resultados no han sido del todo validados y los estudios observacionales con pacientes de práctica clínica habitual tampoco sugieren esta idea. Por lo que las guías internacionales de oncología y onconefrología los siguen considerando de primera línea [38].
o Segunda línea: En caso de persistencia de la proteinuria, nosotros consideramos de segunda línea el uso de iSGLT-2. Si bien es verdad que hoy en día no hay evidencia en este subgrupo de pacientes, se puede extrapolar su beneficio en base a la experiencia en insuficiencia renal crónica diabética o incluso de otras glomerulopatías [52]. Otros agentes antiproteinúricos que se pueden emplear incluyen los antialdosterónicos o diuréticos tiazídicos, teniendo la precaución, como siempre, del riesgo de hipovolemia en pacientes con cáncer.
· Manejo de la Proteinuria Grave, AKI o MAT. La proteinuria severa (rango nefrótico, MAT o AKI) generalmente requiere la interrupción del tratamiento y, como comentábamos en el apartado previo, estaría indicada la biopsia renal. Un esquema orientativo sería el siguiente:
• Proteinuria > 2 /día: Se puede considerar la suspensión temporal del VEGFi hasta que disminuya a < 2 g/día, y reanudar con dosis reducida, habiendo optimizado a la vez el tratamiento antiproteinúrico.
• Proteinuria > 3.5 g/día (Grado 3), Síndrome Nefrótico o MAT: Normalmente en estos casos la suspensión del fármaco es definitiva, pero en caso de recuperación del cuadro se podría revalorar la introducción individualizando caso a caso. Como comentábamos previamente, la mayoría de los casos mejoran o revierten al suspender el fármaco.
• Tratamiento de la MAT: En casos de MAT inducida por VEGFi (especialmente bevacizumab) que no se resuelve con la retirada del fármaco y el control de la PA, el bloqueo del complemento mediante eculizumab (un inhibidor de C5) podría ser una opción, a pesar de que los reportes en la literatura son escasos [53][54].
Reflexión final
En general, en la práctica clínica suele ser un reto el decidir si mantener, suspender o matizar la dosis del tratamiento. Los casos más drásticos son fáciles de reconocer y no generan dudas, por ejemplo, complicaciones hipertensivas graves o insuficiencia renal con requerimiento de diálisis. Pero en la mayoría de las ocasiones el problema suele ser matizable y la decisión depende del correcto balance riesgo-beneficio: si hay opciones alternativas del tratamiento oncológico o el VEGFi es su última opción, la voluntad del paciente, etc. La realidad, en nuestra experiencia, es que muchos pacientes continúan con el VEGFi a pesar de presentar hipertensión o proteinuria, y muchas veces, aunque sobrepase los 2 gramos o la PA no esté al 100% controlada. Esto suele ser porque precisamente hay una cantidad no despreciable de pacientes con neoplasias avanzadas que este es su único tratamiento para intentar mantener sin progresión la enfermedad y aumentar la supervivencia. Así que, con todo esto, queremos transmitir el mensaje que, aunque haya guías y algunos esquemas de manejo, la onconefrología és la máxima expresión del riesgo-beneficio y del consenso entre especialidades y entre médico-paciente, por lo que cada decisión debe de ser especialmente individualizada.