Fístulas Arteriovenosas Endovasculares (endoAVF)
Introducción
La fístula arteriovenosa quirúrgica (AVF) se considera el acceso vascular de elección para los pacientes en hemodiálisis [1]. Sin embargo, la creación reciente de la fístula arteriovenosa percutánea (endoAVF), mediante dispositivos endovasculares, emerge como posible alternativa a la AVF [2] [3] [4].
Consiste en la creación percutánea de un canal endovascular entre la arteria radial (o cubital) proximal y la vena perforante, que conecta los sistemas venosos superficial y profundo, generalmente unos centímetros por debajo del pliegue del codo. Se realiza en sala de angiografía, precisando sedación consciente y anestesia local [4] [5] [6] [7].
La motivación principal para el desarrollo de la endoAVF ha sido la búsqueda de accesos vasculares que minimicen el trauma quirúrgico y las complicaciones asociadas a la cirugía abierta tradicional.
En 1977 Gracz y Toledo-Pereyra describieron, de forma independiente, técnicas quirúrgicas para crear anastomosis en el antebrazo proximal, utilizando la vena perforante [8] [9]. Estas AVF de antebrazo proximal sentaron las bases conceptuales y anatómicas para el desarrollo de los sistemas endovasculares actuales [4].
En 2015 se publicaron los primeros resultados del sistema EverlinQ de 6 Fr (primera generación de WavelinQ), liderados por Rajan et al. [10], demostrando su viabilidad técnica y en 2017 el estudio NEAT (Novel Endovascular Access Trial), un ensayo multicéntrico, evaluó la seguridad y eficacia del sistema EverlinQ en 60 pacientes, reportando una madurez fisiológica del 87% [11]. Ya en el año 2019 Las guías KDOQI incluyen, por primera vez, la creación endovascular como una técnica novedosa dentro del plan de vida del paciente con enfermedad renal.
Sistemas disponibles para la realización de endoAVF
Actualmente, existen dos sistemas principales que han sido aprobados y comercializados para la creación de endoAVF: WavelinQ y Ellipsys. Ambos sistemas ofrecen una alternativa mínimamente invasiva a la cirugía tradicional [11] [12] [13] (Tabla 1).
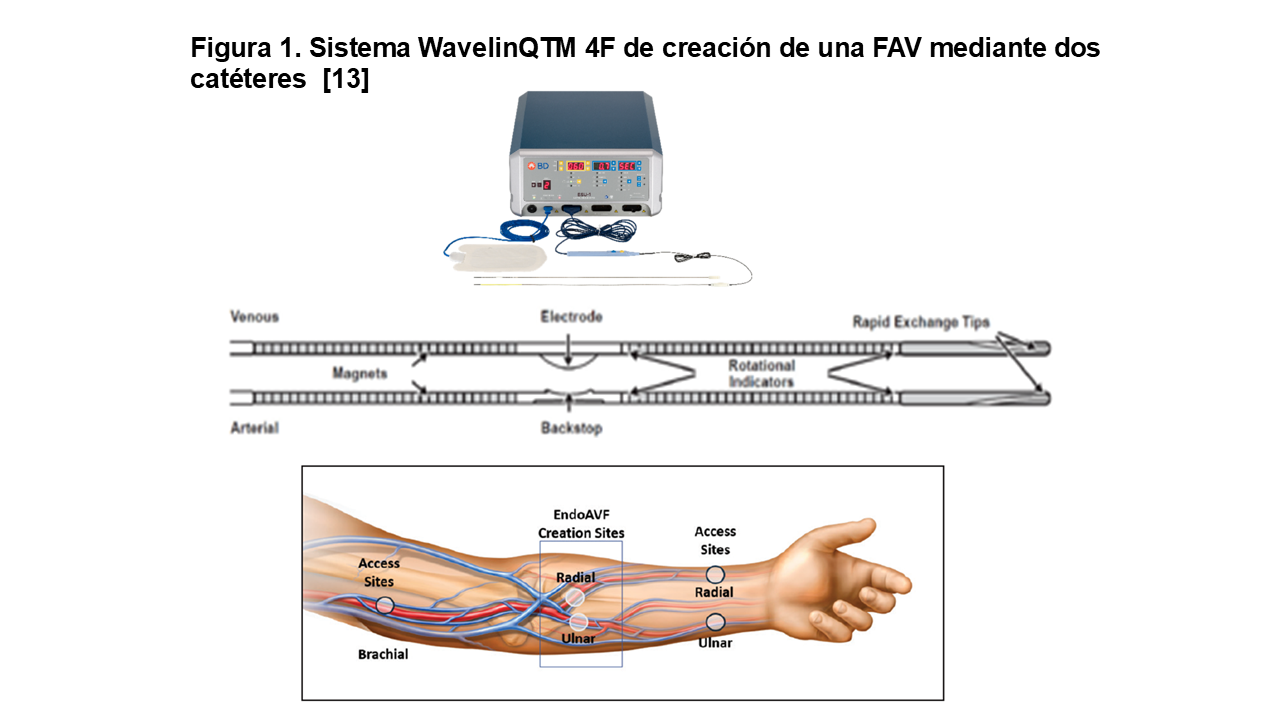
1.Sistema WavelinQ (BD / TVA Medical) (Figura 1)
Es un sistema de doble catéter que utiliza energía de radiofrecuencia para crear la fístula.
• Mecanismo: Se introducen dos catéteres delgados (4 Fr), uno en una arteria y otro en una vena adyacente del antebrazo (radial o cubital). Estos se alinean mediante el uso de imanes.
• Procedimiento: Requiere guía tanto por ecografía (para el acceso inicial) como por fluoroscopia (para posicionar los catéteres).
• Procedimiento adicional: embolización de venas colaterales.
• Tiempo de realización: 60 minutos
• EndoAVF creada: radio-radial o cúbito-cubital en antebrazo proximal
• Evolución: El dispositivo original se conocía como EverlinQ (de 6 Fr), el cual fue reemplazado en 2019 por la versión de segunda generación más pequeña, el WavelinQ 4F. Recibió el marcado CE en Europa en 2014 y en 2018 la aprobación por la FDA.
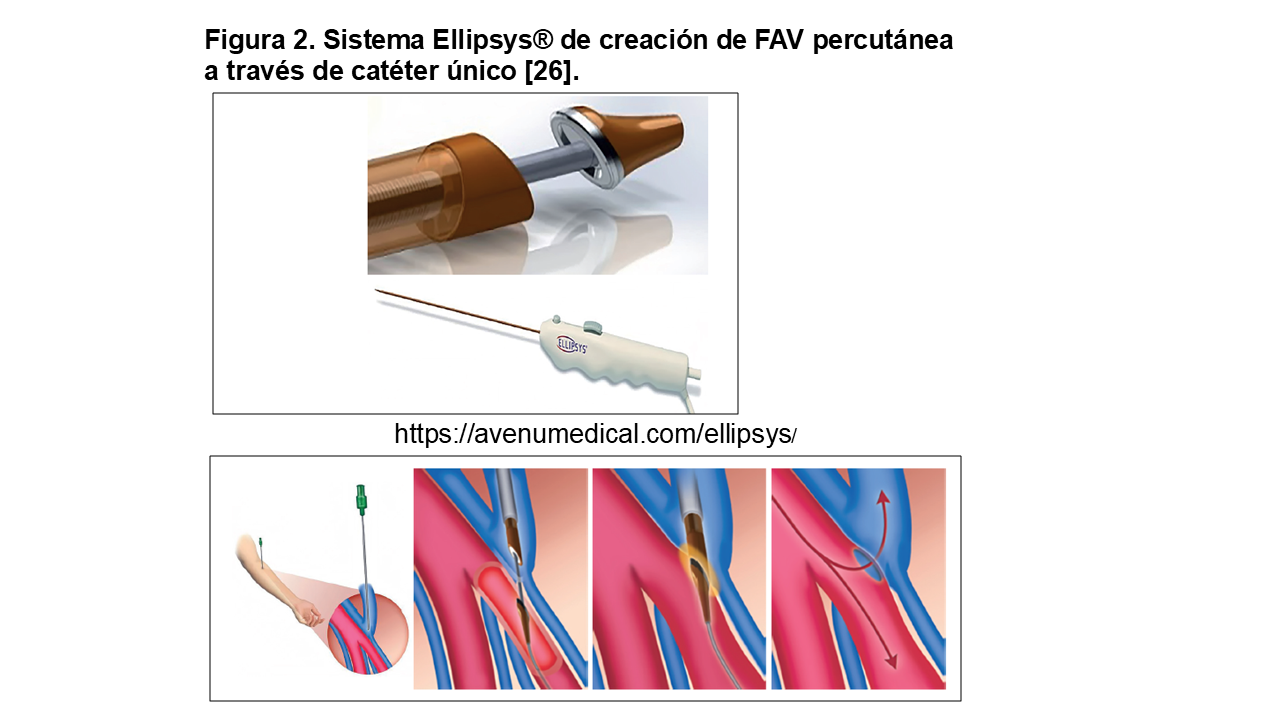
2. Sistema Ellipsys (Medtronic / Avenu Medical) (Figura 2)
Es un sistema de un solo catéter que utiliza energía térmica y presión para fusionar los vasos.
• Mecanismo: El dispositivo se introduce a través de una vena perforante (comunicante profunda) hasta la arteria radial proximal. Al activarse, aplica calor para crear una anastomosis por fusión tisular.
• Procedimiento: Se realiza exclusivamente bajo guía por ecografía, evitando la exposición a radiación o el uso de contraste iodado.
• Procedimiento adicional: angioplastia de la anastomosis.
• Tiempo de realización: 15-30 minutos
• EndoAVF creada: radio-perforante en antebrazo proximal
• Evolución: Recibió el marcado CE en Europa en 2016 y en 2018 la aprobación por la FDA. En la actualidad el sistema Ellipsys ha sido discontinuado y ya no está disponible, desde principios de 2025.
Criterios anatómicos
Ambos dispositivos requieren de la presencia de un sistema arterial indemne, con test de Allen negativo que asegure el flujo por colaterales del arco palmar, y de un drenaje adecuado del sistema venoso superficial a vena cefálica y/o vena basílica. Se elegirá entre uno u otro dispositivo según los requisitos anatómicos indicados en ficha técnica del fabricante [11] [12] [14] (Tabla 2).
Contraindicaciones y Exclusiones
La creación de una endoAVF no debe intentarse en las siguientes circunstancias:
• Calcificación arterial: Presencia de calcificación transmural severa que limite el flujo o impida la compresión del vaso durante la ecografía.
• Trombosis venosa: Venas cefálica o basílica trombosadas o evidencia de oclusión venosa central ipsilateral.
• Limitaciones de flujo: Pacientes con limitaciones severas de flujo arterial o venoso.
• Otras condiciones: Coagulopatía no corregible, infecciones activas en el sitio del procedimiento o insuficiencia cardíaca congestiva severa que pueda verse agravada por la fístula.
Maduración de la endoAVF
La maduración de una endoAVF se determina mediante una combinación de hallazgos ecográficos hemodinámicos (maduración fisiológica) y el éxito clínico en su uso para la diálisis (maduración clínica) [7] [13] [14] [15] (Tabla 3).
1. Maduración Fisiológica
La definición más aceptada de maduración fisiológica se define por el cumplimiento de criterios anatómicos y de flujo específicos, medibles mediante ecografía Doppler.
• Criterios de medición: aunque no existen estándares universales para las endoAVF, se suelen considerar los siguientes parámetros:
o Flujo volumétrico (Qa): Superior a 500-600 mL/min, medido en la arteria braquial de entrada. Algunos protocolos consideran óptimo un flujo de entre 800 y 1000 ml/min.
o Diámetro de la vena: Un diámetro de la vena objetivo superior a 5 mm. Cuando la vena es superficial o se va a canular con eco, puede ser suficiente con un diámetro superior a 4mm.
o Flujo en la vena objetivo: Flujos superiores a 300 mL/min en la zona de punción. Algunos protocolos consideran óptimo un flujo superior a 500ml/min.
o 6 mm de profundidad (distancia desde la superficie de la piel).
o 6 cm de longitud en el segmento apto para la zona de canulación.
• Regla de los 6: Históricamente se ha mencionado la "regla de los 6" (6 semanas, 6 mm de diámetro/profundidad y 600 mL/min de flujo), pero no hay evidencia científica sólida que respalde este estándar para las endoAVF.
• Integridad del circuito: El acceso debe estar libre de estenosis significativas o trombosis.
2. Maduración Clínica
La maduración se considera completa cuando el acceso puede utilizarse de forma rutinaria en hemodiálisis:
• Canulación exitosa: Se define como la capacidad de realizar la diálisis utilizando dos agujas.
• Uso sostenido: El criterio de "usabilidad funcional" requiere que la endoAVF se canule con dos agujas en al menos dos tercios (67%) de las sesiones de diálisis prescritas durante un periodo continuo de 4 semanas.
3. Factores que facilitan la maduración
Para alcanzar estos criterios, es frecuente que las endoAVF requieran procedimientos adicionales, durante su creación, como la embolización de venas colaterales para redirigir el flujo hacia las venas superficiales, especialmente en el sistema WavelinQ o angioplastias de la anastomosis, especialmente en el sistema Ellipsys.
Monitorización de la endoAVF
Es un proceso continuo que comienza inmediatamente después de su creación y se extiende durante toda la vida útil del acceso. Combina la exploración física con la ecografía Doppler para asegurar la maduración adecuada y detectar precozmente cualquier disfunción [7] [14] [15]:
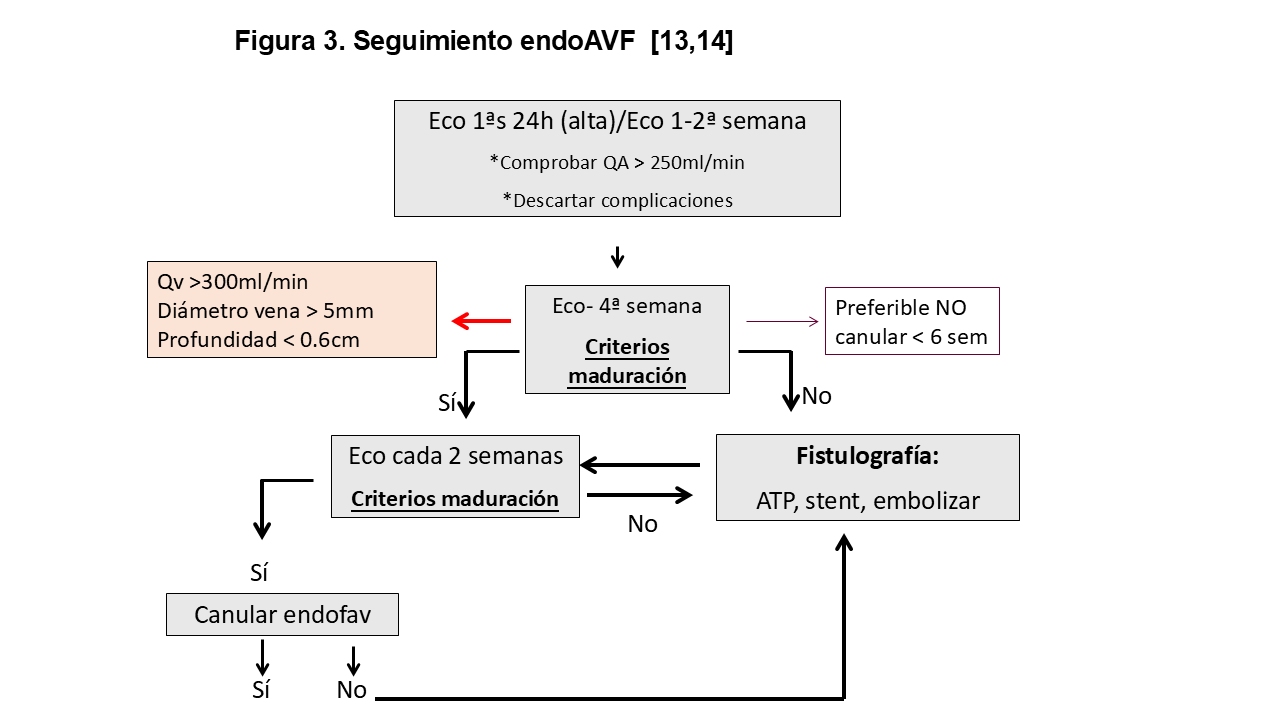
Cronograma de Seguimiento (Figura 3)
• 24 horas tras la creación (antes del alta): valorar la presencia de frémito o soplo. Qa debe ser superior a 250ml/min.
• Primera revisión (entre 7-15 días): se realiza un examen físico inicial y una evaluación ecográfica para confirmar la permeabilidad de la anastomosis y detectar problemas tempranos, como pequeños trombos o pseudoaneurismas. El Qa debe ser superior a 250ml/min
• Evaluación crítica (4 semanas): Es el hito fundamental para determinar si la fístula ha madurado. Si en este punto no se cumplen los criterios de maduración es poco probable que la fístula madure por sí sola y se deben programar intervenciones secundarias.
• Seguimiento a largo plazo: Una vez establecida, se recomiendan evaluaciones periódicas a los 3, 6, 9 y 12 meses para monitorizar el Qa y la evolución de las venas de salida.
Algoritmo de Intervención en el Seguimiento (Figura 4)
Se aplicará un protocolo de intervención en caso de detectar fallo en la maduración o la presencia de disfunción a largo plazo [7] [12] [14] [15]:
• Si el Qa es bajo (fallo de maduración Tipo 1): se buscará una estenosis. El tratamiento suele ser la angioplastia transluminal percutánea (ATP) de la anastomosis, de la vena comunicante profunda o de la arteria radial pre-anastomótica.
• Si el Qa es adecuado, pero no llega a la vena superficial (fallo de maduración Tipo 2): el flujo puede estar desviándose hacia el sistema venoso profundo. En este caso, el seguimiento deriva en procedimientos de redirección de flujo, como la embolización con coils de venas competitivas (por ejemplo, la vena braquial o la vena cubital mediana) para forzar el paso de sangre hacia la vena cefálica.
• Durante el seguimiento a largo plazo se indicará una intervención endovascular de mantenimiento cuando se objetiven datos ecográficos o clínicos de disfunción, al igual que en la AVF.
Complicaciones endoAVF
La creación de endoAVF presenta un perfil de seguridad favorable, con una tasa global de complicaciones que oscila entre el 5,46% y el 10% según diversos estudios [6] [12] [16].
Relacionadas con el procedimiento:
• Espasmo vascular
• Hematomas
• Disección de la arteria braquial o venosa
• Trombosis intraprocedimiento
• Pseudoaneurisma
• Migración de coils durante la embolización
• Extravasación de contraste.
Complicaciones Vasculares Comunes
• Trombosis precoz y tardía: Es una de las complicaciones más reportadas, con una incidencia de aproximadamente el 9% al 11%. La trombosis suele ser la causa principal de abandono del acceso en el primer año.
• Seudoaneurismas: Se presentan en aproximadamente el 3% al 4% de los casos. Pueden localizarse en el sitio de la anastomosis o en el punto de acceso (punción) braquial o radial.
• Estenosis: Es una causa frecuente de disfunción del acceso que requiere intervención para mantener la permeabilidad.
• Hematomas: Se reportan en alrededor del 9% de los pacientes, generalmente relacionados con el sitio de acceso vascular.
• Neuropatía: Se han reportado casos raros de parestesias transitorias o neuropatía isquémica monomélica, esta última relacionada con el robo arterial y que requiere el cierre inmediato de la fístula.
• Síndrome de robo
Canulación de endoAVF
La canulación de la endoAVF presenta una serie de peculiaridades respecto a la AVF, por ello requiere un enfoque de equipo altamente coordinado y protocolos específicos para lograr que esta sea exitosa. Precisa formación del personal de hemodiálisis en punción eco-guiada y educación exhaustiva del paciente para proteger el acceso [14] [17].
Desafíos en la localización y canulación:
A diferencia de la AVF del brazo superior que utiliza la arteria braquial, la endoAVF utiliza la arteria radial o cubital proximal, lo que resulta en un flujo de bajo a moderado. Aunque este flujo es suficiente para la diálisis, presenta retos específicos:
1. Dificultad de localización: El flujo moderado puede hacer que la fístula sea difícil de palpar inicialmente.
2. Ausencia de cicatrices: La falta de cicatrices quirúrgicas elimina los puntos de referencia tradicionales para el personal de enfermería.
3. Múltiples venas de salida: Debido a la anatomía del sistema venoso profundo y superficial, ocluir la salida con un solo dedo a menudo no es suficiente para distender el vaso. Precisa del uso de un torniquete.
Protocolos de preparación y marcación
El éxito de la primera canulación depende de la confirmación de los criterios de maduración funcional ecográficos por el equipo médico.
Idealmente la primera canulación debe ser ecoguiada. No obstante, en el caso de que no sea posible, el radiólogo intervencionista podrá marcar la zona a canular para facilitar los puntos de punción.
Protocolo de canulación
Puede haber múltiples venas de salida. Precisa torniquete.
Idealmente realizar la punción guiada con ecografía.
Ángulo de 20-35 grados.
Iniciar la punción con agujas de bajo calibre y aumentar gradualmente en el calibre y la tasa de flujo para permitir la maduración y adaptación del vaso (Tabla 4).
A nivel de codo se pueden utilizar agujas canuladas (para evitar posibles rotura de vasos con el movimiento) o en el caso que la vena de punción esté algo más profunda.
Nunca utilizar pinzas (clamps)
Formación del personal de hemodiálisis e intervencionista
La formación del personal es un factor determinante para el éxito y la longevidad de las endoAVF, ya que su manejo clínico y técnica de punción difieren de las AVF [6] [14] [17] [18].
Los puntos clave sobre la formación del personal incluyen:
Necesidad de capacitación específica
• Diferencias en la técnica: La punción de una endoAVF requiere un enfoque distinto al de una AVF. Es esencial que el personal aprenda a manejar estas fístulas, que suelen sentirse más blandas y pueden tener múltiples venas de salida (como la cefálica y la media cubital), lo que permite opciones de punción únicas como la punción dual en venas separadas.
• Identificación del trayecto: Al no presentar cicatrices quirúrgicas ni protrusiones cutáneas evidentes, el personal debe ser entrenado para localizar las zonas de canulación mediante la palpación con torniquete y el uso de guías visuales.
Estrategias de Formación y Apoyo
• Uso de ecografía: Se recomienda encarecidamente que el personal de enfermería realice las primeras punciones guiadas por ecografía. Esta práctica no solo educa al personal sobre la anatomía del acceso, sino que mejora los resultados y reduce el riesgo de complicaciones como la punción de la pared posterior del vaso.
• Marcaje y diagramas: Una estrategia útil para facilitar la transición es que el médico que creó la fístula proporcione diagramas o fotos de las zonas de canulación o realice marcajes físicos en el brazo del paciente tras la evaluación postoperatoria.
• Recursos de la industria: La capacitación técnica puede ser apoyada por especialistas clínicos de las empresas fabricantes de los dispositivos, quienes ofrecen programas de educación dedicados a la canulación de endoAVF.
• Colaboración con el intervencionista: El radiólogo o nefrólogo intervencionista que creó el acceso debe ser el punto de contacto principal para resolver dudas. Se sugiere que estos especialistas visiten las unidades de diálisis para asistir al personal en casos de canulación persistente difícil.
Formación del Personal Médico Intervencionista
Además del personal de enfermería, los médicos que realizan el procedimiento deben cumplir con requisitos de formación estrictos:
• Curva de aprendizaje: Se estima que los operadores requieren entre 5 y 10 procedimientos con cada dispositivo para superar la curva de aprendizaje inicial.
• Requisitos de certificación: Para el sistema WavelinQ, por ejemplo, los centros no pueden adquirir el dispositivo hasta que el médico haya completado un seminario web didáctico, entrenamiento individual con un especialista y la realización de 3 casos simulados y supervisados.
• Habilidades ecográficas: La pericia en la evaluación de la anatomía vascular mediante ecografía Doppler es un requisito previo fundamental antes de intentar la creación de una endoAVF.
Educación del Paciente
La educación debe comenzar desde el momento en que se identifica al paciente como candidato a una endoAVF [6] [14] [17] [18].
Se le deberá instruir en las siguientes recomendaciones:
• Restricciones clínicas: no permitir extracciones de sangre ni toma de presión arterial en el brazo del acceso.
• Evitar compresión: no usar ropa ajustada, mangas apretadas o cargar bolsas de supermercado en el brazo afectado.
• Protección durante el sueño: evitar dormir sobre el brazo del acceso para prevenir oclusiones y coágulos.
• Evaluación diaria: el paciente debe aprender a palpar el acceso diariamente y, de ser posible, usar un estetoscopio para escuchar la anastomosis.
• Durante la diálisis: mantener el brazo inmóvil y en una posición cómoda que sea visible para el equipo clínico.
Selección de pacientes para la creación de endoAVF
La selección de pacientes es un proceso exhaustivo que combina criterios clínicos, anatómicos y de planificación de vida [14].
Los puntos clave para la selección de pacientes son los siguientes:
Paciente cuya expectativa de vida supera el año.
Con anatomía favorable.
Negativa a la cirugía o contraindicación para la misma.
Pacientes candidatos a AVF radiocefálica (AVFr-c), pero con riesgo de mala cicatrización (diabéticos, obesos, frágiles, anticoagulados).
No candidato a AVFr-c o con AVFr-c previa no funcionante. Es importante destacar que la creación de una endoAVF no impide la posibilidad de realizar una AVF radiocefálica distal en el futuro si fuera necesario.
La obesidad no es una contraindicación: contrario a lo que se podría pensar, la obesidad por sí sola no es un factor limitante. De hecho, el sistema venoso suele estar mejor preservado en pacientes obesos al haber sufrido menos punciones previas.
Antes que la realización de una AVF protésica.
Considerarla en aquellos pacientes con cardiopatía moderada.
Urgencia: Puede ser una excelente opción para pacientes que se acercan rápidamente a la necesidad de diálisis, ya que un programa bien organizado puede realizar el mapeo y la creación en una semana, logrando la canulación aproximadamente 4 semanas después.
También habrá que tener en cuenta las siguientes consideraciones:
Apoyo quirúrgico: una contraindicación absoluta para la endoAVF es la falta de apoyo quirúrgico, ya que las venas diana pueden requerir procedimientos secundarios como superficialización.
Hemodiálisis domiciliaria (HDD): la elección por parte del paciente de HDD se puede considerar como contraindicación relativa, teniendo en cuenta que la canulación de la endoAVF suele presentar mayor dificultad. Dependerá sobre todo de las características anatómicas del paciente.
Formación adecuada del equipo de profesionales implicados en su realización, canulación y seguimiento.
Educación adecuada del paciente.
Importancia del Equipo Multidisciplinario:
El éxito de la selección reside en la colaboración entre nefrólogos, radiólogos intervencionistas y cirujanos vasculares. El nefrólogo suele liderar la identificación de candidatos basados en su historia clínica, mientras que el especialista intervencionista realiza el mapeo preciso para asegurar la viabilidad técnica y seleccionar el dispositivo más adecuado según la anatomía del paciente.
Resultados de la endoAVF
Los resultados globales de la creación de endoAVF indican que es una técnica eficaz y segura, con altas tasas de éxito técnico y permeabilidad a largo plazo (Tabla 5).
Los datos comparativos entre la endoAVF y la AVF sugieren resultados equiparables. Aunque las AVF pueden ofrecer mayores tasas de permeabilidad primaria, las endoFAV mantienen una permeabilidad secundaria aceptable y un perfil de complicaciones reducido, con menor incidencia de isquemia distal. Se han objetivado ventajas en tiempos quirúrgicos y costes, mientras que los resultados de maduración e intervenciones varían según los estudios [5] [16] [19] [20] [21] [22] [23].
Cuando se comparan ambos dispositivos, Ellipsys destaca por su rapidez en madurar, mayor permeabilidad secundaria y menor tasa de fallo definitivo, mientras que WavelinQ ofrece la ventaja de requerir menos procedimientos de mantenimiento a corto plazo, aunque a riesgo de una mayor tasa de abandono total del acceso [5] [11] [24] [25] [26].
Posibles ventajas de endoAVF
• Opción para los pacientes que se niegan a cirugía
• Proporciona más opciones anatómicas incrementando las posibilidades de AV del paciente.
• Preservación de vasos: esta técnica permite utilizar la vasculatura del antebrazo proximal, preservando los vasos del brazo superior para posibles accesos futuros en caso de fallo.
• Menor tasa de complicaciones: presentan un riesgo significativamente inferior de sufrir infecciones de la herida y síndrome de robo arterial.
• Reducción de morbilidad: el uso de la arteria radial proximal como flujo de entrada permite un control más efectivo del flujo, disminuyendo el riesgo de insuficiencia cardíaca de alto gasto y de neuropatía isquémica monomélica.
• Menor lesión endotelial: lo cual puede mejorar la permeabilidad primaria y disminuir la tasa de fallo primario
• Menos aneurismas: presentan una menor tendencia a la degeneración aneurismática a largo plazo.
• Zona de canulación extendida: al no haber cicatrices quirúrgicas y distribuir el flujo a través de múltiples venas de salida (como la cefálica, basílica y media cubital), se amplía el área disponible para la punción.
• Anastomosis profunda por lo cual su punción accidental sería improbable.
• Entorno ambulatorio: el procedimiento suele realizarse en salas de angiografía sin necesidad de quirófano ni anestesia general, facilitando el alta el mismo día.
• Rapidez en la creación: un programa eficiente puede realizar el mapeo y la creación del acceso en una semana, logrando la canulación exitosa en aproximadamente 4 semanas.
• Diversidad de operadores: expande el grupo de especialistas que pueden crear accesos vasculares, incluyendo radiólogos y nefrólogos intervencionistas, además de cirujanos vasculares.
• Ahorro de costes.
• Estética superior: La ausencia de cicatrices visibles y el aspecto más discreto del brazo mejoran la satisfacción y aceptación del paciente, reduciendo el impacto psicológico del acceso vascular.
• Menor dolor: al evitar incisiones extensas, los pacientes reportan menos dolor postoperatorio.
Desventajas de endoAVF
Requisitos anatómicos estrictos: sólo el 50-69% de los pacientes evaluados suelen cumplir con los criterios anatómicos necesarios
Precisa de personal intervencionista entrenado y disponibilidad de sala de angiografía.
Alta tasa de reintervenciones correctivas para la maduración: embolización de venas competitivas y angioplastias.
Curva de aprendizaje en la canulación y manejo clínico del personal de hemodiálisis.
Coste inicial elevado.
Experiencia en nuestro Centro
En nuestro centro, durante los últimos 5 años, se han realizado 26 endoAVF con resultados aceptables.
Características de los pacientes (Tabla 6):
Pacientes del área norte de la isla de Tenerife
19 varones y 7 mujeres
Edad media 59 años (rango 16-79)
La indicación principal: presentar fístulas previas no funcionantes (favNF).
Presencia de factores de riesgo para el acceso vascular: 58% diabéticos, 26% con IMC > 30, 27% con enfermedad vascular periférica, 20% con trombosis de venas centrales y 58% con favNF.
Características del procedimiento
Valoración ecográfica previa de criterios anatómicos aptos.
Realizado por Radiología Intervencionista.
Se emplearon 23 dispositivos WavelinQ y 3 dispositivos Ellipsys.
El 60% de los pacientes precisaron intervención adicional durante el procedimiento: 4 angioplastias (ATP), 3 embolizaciones y en 5 ambos.
Complicaciones durante el procedimiento en 5/26 (19%): 4 hematomas leves, 1 vasoespasmo, 1 hemorragia severa.
Resultados (Tabla 7) (Tabla 8) (Figura 5)
Tiempo medio de seguimiento: 747 ± 396 días (150-1445 días)
Parámetros de eficacia
o Éxito técnico del 92%
o Fallo primario en 23%
o Maduración fisiológica a los 90 días del 60%.
o Maduración fisiológica a los 150 días del 80%.
o Permeabilidad 1ª a los 12 meses: 65%.
o Permeabilidad acumulada a las 12 meses: 84%.
o Criterios de usabilidad en el 65%.
Parámetros de seguridad
o Intervenciones correctivas 1,91 paciente/año.
o Intervenciones de mantenimiento 1,2 paciente/año.
o % abandono: 35%.
En nuestros pacientes el éxito inicial de la técnica fue elevado (92%), aunque se objetivó un fallo primario del 23%. No se observaron complicaciones graves. El 50 % de los pacientes precisaron reintervención endovascular para su maduración o mantenimiento. Aunque el tiempo medio de maduración y usabilidad y la tasa de intervenciones endovasculares fue mayor al descrito en la literatura, la permeabilidad acumulada a los 24 meses se mantuvo en el 84% de los pacientes.
En nuestra experiencia la endoAVF supuso una alternativa exitosa y segura para pacientes con anatomía compleja y con factores de riesgo relacionados con malos resultados de la AVF.
Reflexiones
Recientemente la actualización 2025 de la Guía Clínica Española del Acceso Vascular para Hemodiálisis, después de hacer una revisión sistemática de la literatura, recomienda no utilizar la endoFAV como alternativa generalizada a la FAV quirúrgica convencional en el paciente candidato a hemodiálisis (Recomendación condicional) [27].
En nuestro centro la endoAVF está integrada en la actividad asistencial del Servicio de Radiología Intervencionista, desde noviembre de 2019, y aunque la consideramos como una opción en nuestro algoritmo de “individualización de la indicación del acceso vascular” (Figura 6), hasta el momento seguimos planteando la AVF como primera elección.
Tal y como se refleja en la literatura, el éxito de la técnica va a depender de varios factores: anatomía favorable del paciente, recursos y formación del personal médico y de las unidades de hemodiálisis y de un programa de seguimiento exhaustivo. En este sentido, tuvimos que superar varias barreras para construir el proceso de la endoAVF. Concretamente llevamos a cabo varias acciones:
Los Radiólogos Intervencionistas recibieron formación para el dispositivo WavelinQ con entrenamiento individual con un especialista y los primeros 5 casos fueron supervisados.
Se instruyó al personal de enfermería en su canulación y en el manejo ecográfico.
Se creó circuito con las unidades de hemodiálisis extrahospitalarias iniciando la canulación en la unidad hospitalaria. Una vez que se cumplían criterios de usabilidad, el paciente se trasladaba a su unidad correspondiente. También se instruyó al personal de esas unidades.
Formación del nefrólogo de la unidad hospitalaria en seguimiento ecográfico de la endoAVF para realizar las revisiones semestrales.
Colaboración entre nefrólogos, radiólogos intervencionistas y cirujanos vasculares. El nefrólogo suele liderar la identificación de candidatos basados en su historia clínica, mientras que el especialista intervencionista realiza el mapeo preciso para asegurar la viabilidad técnica y seleccionar el dispositivo más adecuado según la anatomía del paciente.
Si bien, nuestros resultados fueron aceptables, encontramos varias áreas de mejora dentro del proceso de la endoAVF:
El cumplimiento estricto de los criterios anatómicos va unido al éxito de la técnica. En nuestro caso asumimos a pacientes con criterios límite, incluso con síndrome de vena cava superior o trombosis de venas centrales repermeabilizadas. Aun así, los pacientes obtuvieron beneficios con la endoAVF.
Cuando la vena que se desarrolla es la basílica, por lo general, se tarda más en adquirir la madurez fisiológica. Suele estar profunda y muy cerca de la arteria humeral, lo que aumenta el riesgo de la punción arterial al intentar canular la endoAVF. Actualmente en nuestro protocolo sólo estamos asumiendo pacientes con valoración ecográfica previa con buen drenaje por vena cefálica, y si fuera por la vena basílica, sólo en aquellos con brazos delgados cuya profundidad a la piel sea menor de 6 mm.
Se recomienda realizar las primeras canulaciones ecoguiadas. Esto conlleva problemas logísticos de personal, que retrasan la madurez clínica de la endoAVF. Es muy importante formar al personal de enfermería en la punción ecoguiada y también al personal médico como apoyo.
Problemas de sobrecarga asistencial en la unidad hospitalaria pueden retrasar el inicio de la canulación de pacientes de Unidades extrahospitalarias y retrasar por ello en la maduración clínica. Mejorar este circuito mejorará los resultados clínicos de los pacientes.
La endoAVF podría tener beneficios, entre otros, en 2 perfiles de pacientes, 1) como RESCATE de aquellos con anatomía marginal o con fracaso previo de accesos distales, y 2) como URGENCIA DE TIEMPO en aquellos con anatomía óptima, sin factores de riesgo, a los cuales interesa ganar tiempo y asegurar el éxito del AV.
Futuro
En definitiva, la endoFav puede representar una opción más para el paciente. La decisión de crear una endoFAV frente a una AVF debe individualizarse discutiendo las expectativas y preferencias del paciente, las comorbilidades, la anatomía vascular, la integridad de la piel y la experiencia y disponibilidad del equipo profesional [28].
Actualmente, el sistema WavelinQ 4F sigue siendo la opción predominante disponible comercialmente. Se están investigando nuevos dispositivos que buscan simplificar aún más el procedimiento y acelerar la maduración funcional.
En resumen, la endoAVF es una técnica altamente dependiente de la anatomía del paciente y de la pericia del equipo médico, requiriendo un seguimiento estrecho y, a menudo, intervenciones adicionales para asegurar su funcionalidad.