Ecografía pleuropulmonar del paciente renal
La valoración del paciente con disnea es uno de los problemas más frecuentes que nos encontramos en la práctica clínica y, a pesar de esto, en muchas ocasiones no resulta factible realizar un diagnóstico rápido y claro que nos permita un tratamiento adecuado y oportuno. Esto se explica en parte por la gran comorbilidad que presentan muchos de nuestros pacientes y por la falta de medios diagnósticos precisos en el momento de la valoración. En el presente capítulo abordaremos la utilidad de la ecografía pleuropulmonar como herramienta no invasiva, accesible y rentable en el manejo del paciente renal con disnea.
Líquido pulmonar extravascular
El líquido pulmonar extravascular o edema pulmonar es la cantidad de agua que está contenida en los pulmones fuera de la vasculatura pulmonar y corresponde a la suma de los líquidos intersticial, alveolar, intracelular y linfático. Se relaciona con la presión de llenado del ventrículo izquierdo, que es un biomarcador establecido para la estratificación de riesgo cardiovascular y muerte.
La valoración del agua pulmonar extravascular puede servir para la prescripción y monitorización de la terapia con fluidos en pacientes de alto riesgo y se puede medir directamente mediante el método de termodilución transpulmonar o indirectamente por ecografía.
Instrumentos de valoración de la congestión pulmonar
Hay numerosos instrumentos que pueden ayudar en la valoración del edema pulmonar. Entre ellos se encuentran:
- Clínica, que no es específica y, a menudo, aparece de manera tardía.
- Auscultación, poco sensible y poco específica.
- Radiografía de tórax, equívoca y tardía en muchos casos.
- Tomografía axial computarizada (TAC) torácica, técnica compleja y poco reproducible debido a la emisión de radiaciones ionizantes.
- Medición de la presión de enclavamiento de la arteria pulmonar (PCP) mediante catéter de Swanz-Ganz, técnica invasiva solo disponible en las unidades de cuidados intensivos.
- Medición del BNP (péptido natriurético cerebral), de escasa utilidad en la enfermedad renal.
- El estudio del tejido pulmonar mediante biopsia o autopsia.
Valorando los instrumentos anteriores y teniendo en cuenta que los métodos sencillos son poco sensibles y los métodos sensibles son muy complejos, es necesaria una técnica que aúne sensibilidad y sencillez y estas dos características las reúne la ecografía pleuropulmonar, herramienta hoy en día al alcance de todos.
Indicaciones de la valoración ecográfica pleuropulmonar
Diagnóstico preclínico de la congestión pulmonar.
Apoyo en el diagnóstico clínico de la disnea y/o insuficiencia respiratoria
Evaluación de la respuesta al tratamiento pautado (depletivo/volumen).
Prevención de la sobrecarga de volumen en pacientes cardiópatas.
Diagnóstico diferencial de derrame pleural.
Diagnóstico y seguimiento de procesos neumónicos.
Tromboembolismo pulmonar.
Neumotórax.
Guía para procedimientos invasivos: toracocentesis
Aparataje para la ecografía pleuropulmonar
Necesitaremos un ecógrafo convencional con al menos dos sondas, una de baja y otra de alta frecuencia.
La sonda de alta frecuencia o lineal (5-13mHz) es útil para ver estructuras superficiales (hasta 4 cm) y la sonda de baja frecuencia o convexa (3-5 mHz) nos permitirá ver estructuras profundas (hasta 20-30 cm) según la gama del equipo. Si disponemos de ella, la sonda micro-convex (empleada en ecocardiografía) será de utilidad para ver estructuras profundas de difícil acceso, ya que su tamaño es muy inferior a la convex abdominal y podemos introducirla con facilidad en los espacios intercostales.
Ecografía pleuropulmonar: patrón normal
El pulmón, al tratarse de un órgano aireado, no se ha considerado susceptible de valoración mediante ecografía, ya que el aire no transmite bien las ondas ultrasónicas [1].
Por ello, la valoración pulmonar de los enfermos se ha basado históricamente en la utilización de técnicas radiológicas como la radiografía simple y la TAC, empleando ambas radiaciones ionizantes.
Los ultrasonidos son reflejados por el hueso y el aire del parénquima pulmonar, de tal forma que estas estructuras se comportan como una verdadera barrera acústica que impide el paso del haz ultrasónico a través de ellas, produciendo un gran artefacto. Sin embargo, cuando el pulmón está ocupado por agua o el parénquima presenta una consolidación se generan imágenes anómalas que pueden ser percibidas y valoradas mediante ecografía. Es decir, la ecografía pulmonar consiste en interpretar determinados artefactos ecográficos ya que el pulmón no se puede ver.
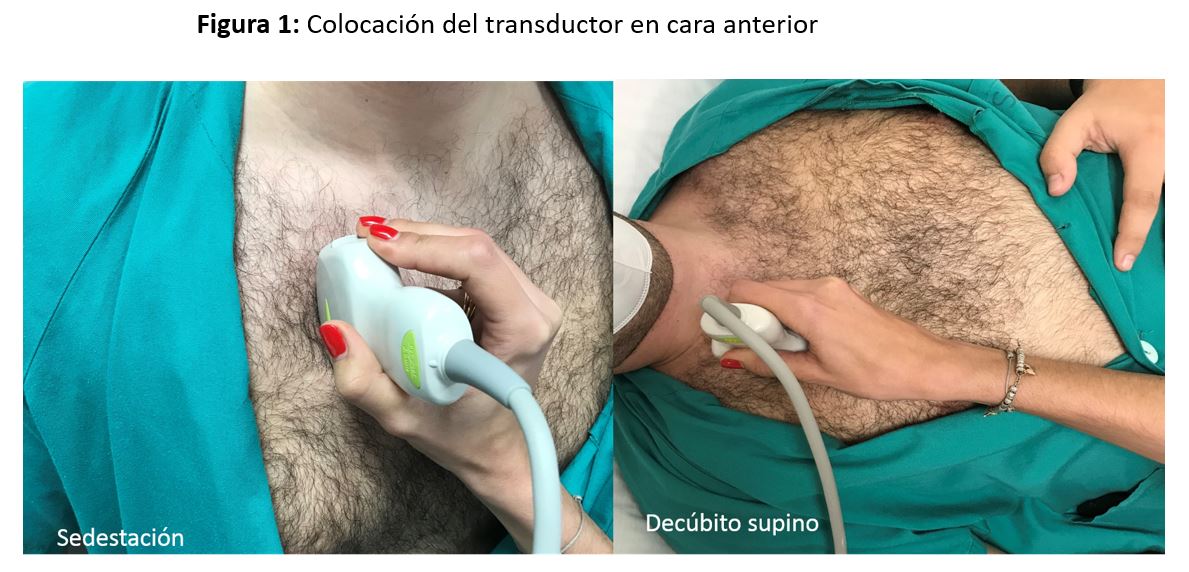
La exploración se inicia con el paciente sentado o en decúbito supino, situando la sonda en sentido longitudinal al tórax y transversal a los espacios intercostales. Iniciaremos la exploración a nivel del 2º espacio intercostal (debajo de la clavícula), realizando un barrido de cada espacio intercostal desde el ápex hasta la base y el diafragma, haciendo lo mismo al abordar las áreas posteriores (Figura 1).
En la exploración ecográfica del pulmón de un individuo sano podemos distinguir:
Deslizamiento pleural o sliding
Al realizar el estudio ecográfico pulmonar de una persona sana se puede distinguir claramente la pleura o línea pleural y el deslizamiento de ambas pleuras (parietal y visceral) con los movimientos respiratorios, conocido ecográficamente como deslizamiento pleural o sliding. Tiene especial interés ya que la ausencia de éste hace sospechar neumotórax, atelectasia o adherencias pleurales [2].
Líneas A
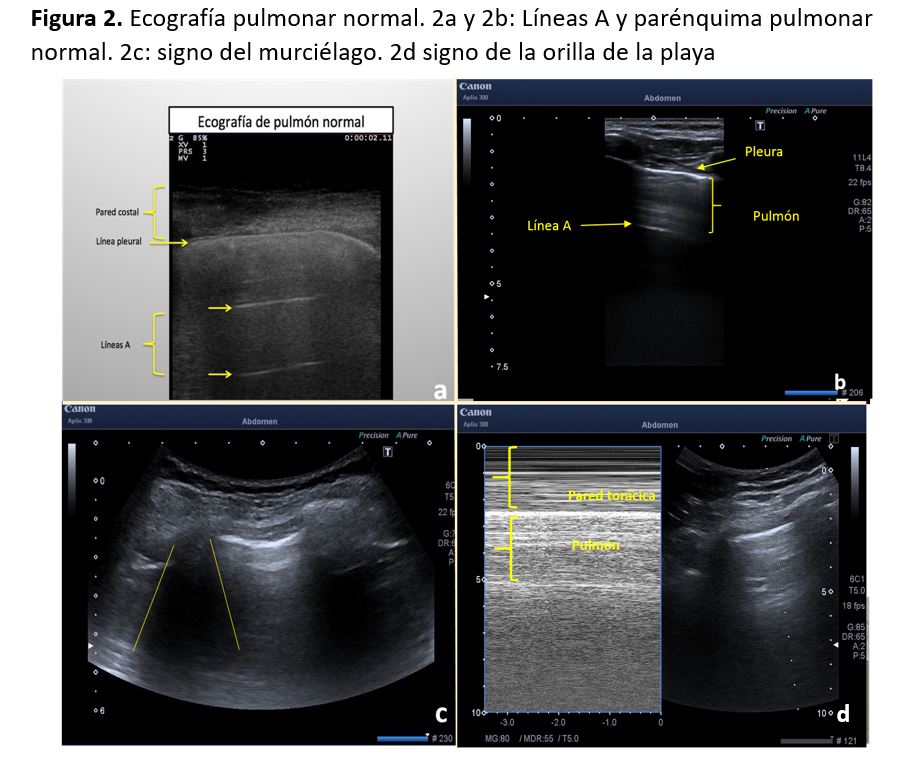
Se trata de líneas hiperecogénicas horizontales paralelas que representan un artefacto de reverberación que se repite de forma más o menos equidistante y paralelas a la línea pleural (Figura 2)a y (Figura 2)b.
En resumen, el signo del deslizamiento pleural, la línea pleural y las líneas A representan un patrón ecográfico pulmonar normal y son fisiológicas. Un patrón ecográfico normal con presencia de líneas A excluye la posibilidad de un edema de pulmón [3].
Signo del murciélago
Con la sonda convex en posición perpendicular a las costillas observaremos en el centro el pulmón y las pleuras, y en los laterales unas sombras acústicas generadas por las costillas. Estas sombras se denominan alas del murciélago y también se trata de un signo fisiológico (Figura 2)c. Con la sonda lineal este signo está presente aunque es menos evidente.
Signo de la arena de playa o sea "shore sign"
Dado que un pulmón normal se encuentra principalmente lleno de aire, al colocar la sonda se produce una reverberación de los ultrasonidos que genera una imagen moteada. Con la sonda lineal en modo M podemos observar dos zonas diferenciadas: la parte superficial representa la pared torácica (el mar) y la inferior el parénquima pulmonar (arena de la playa). Ambas zonas están divididas por una franja blanca que es la pleura (Figura 2)d.
Ecografía del edema pulmonar
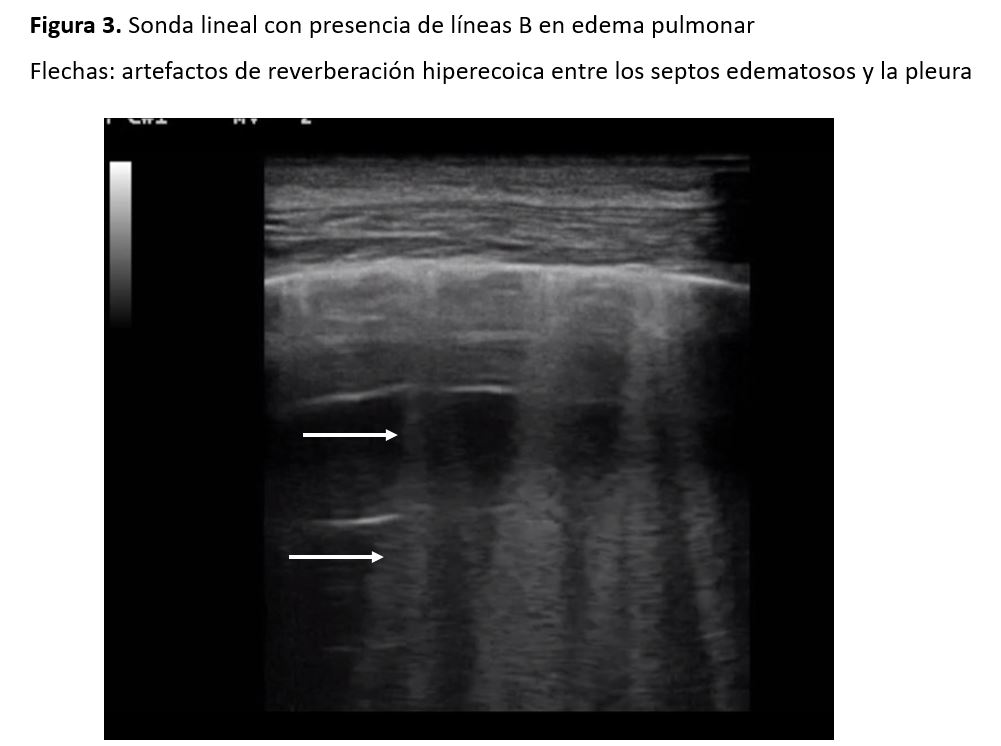
Las líneas B o cohetes pulmonares son líneas hiperecogénicas verticales a modo de láser, de base estrecha, que van desde la pleura hasta la base de la pantalla, se movilizan con la respiración y pueden llegar a borrar las líneas A, generando un patrón característico de "pulmón blanco". La racionalidad de esta técnica es que en presencia de congestión pulmonar el haz de ultrasonidos se refleja en los septos interlobulares, lo que genera artefactos de reverberación hiperecoica entre los septos edematosos y la pleura [2][4] (Figura 3).
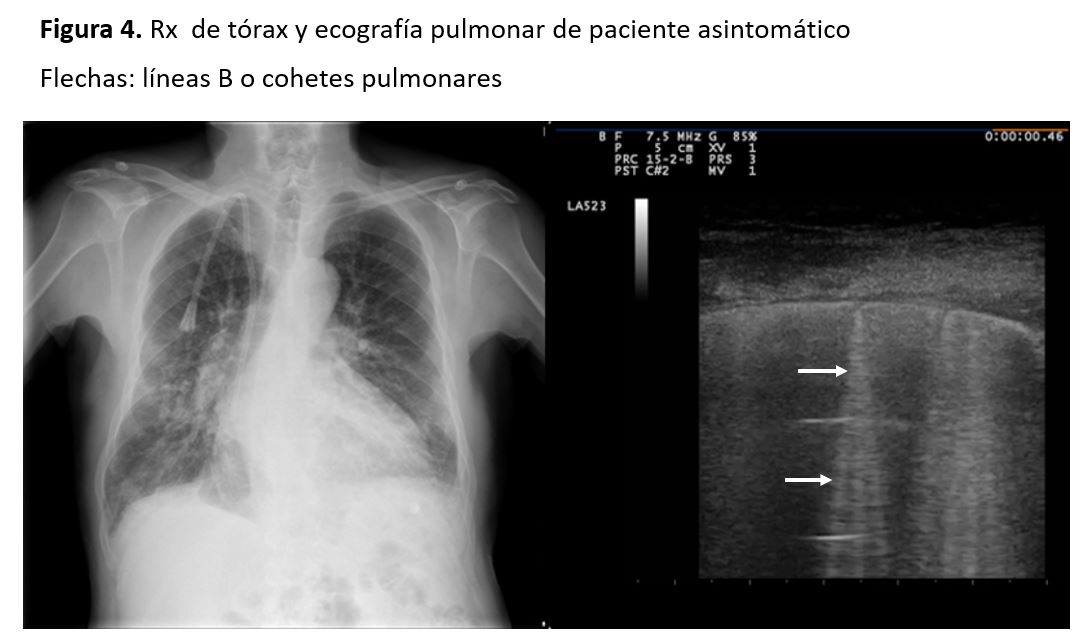
Estos haces se relacionan con la presión de llenado del ventrículo izquierdo y permiten la evaluación del agua pulmonar extravascular, aunque también se pueden encontrar en la fibrosis pulmonar y en el síndrome de distrés respiratorio [4] [5] [6]. El número, grosor y la confluencia de líneas se relacionan con la intensidad del edema. La aparición de estos signos tiene una sensibilidad del 100% y viceversa, siempre que sean difusos en ambos campos pulmonares. Son de aparición precoz y se ven con frecuencia en pacientes con radiografía de tórax normal y/o asintomáticos (Figura 4).
Las líneas B son un fenómeno dinámico que varían rápidamente con los cambios del agua pulmonar extravascular. La evolución de las líneas B nos permite medir en tiempo real la respuesta al tratamiento deplectivo con diuréticos o la respuesta a la ultrafiltración (UF) [7][8].
Técnica del estudio del edema pulmonar
Para la valoración del edema pulmonar mediante ecografía se puede realizar la exploración con el paciente en decúbito supino (si tolera) o sentado. Emplearemos la sonda lineal o de alta frecuencia (7.5-12 MHz) para el ápex pulmonar y la convex o de baja frecuencia (2-5 MHz) para estructuras más profundas (> 6cm), con los modos ecográficos B y M, no siendo necesario el estudio Doppler.
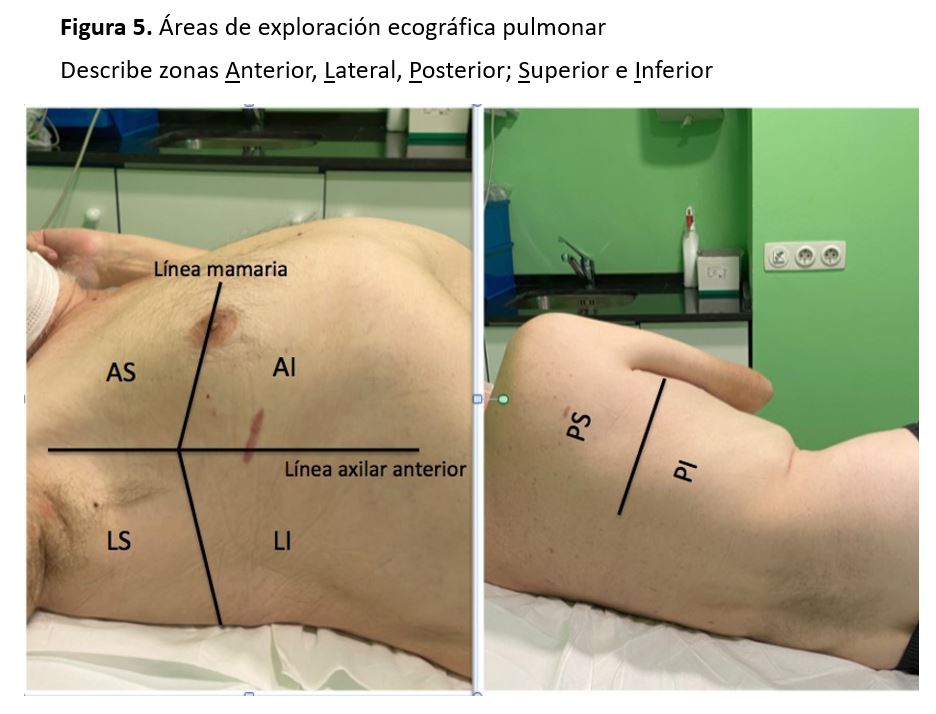
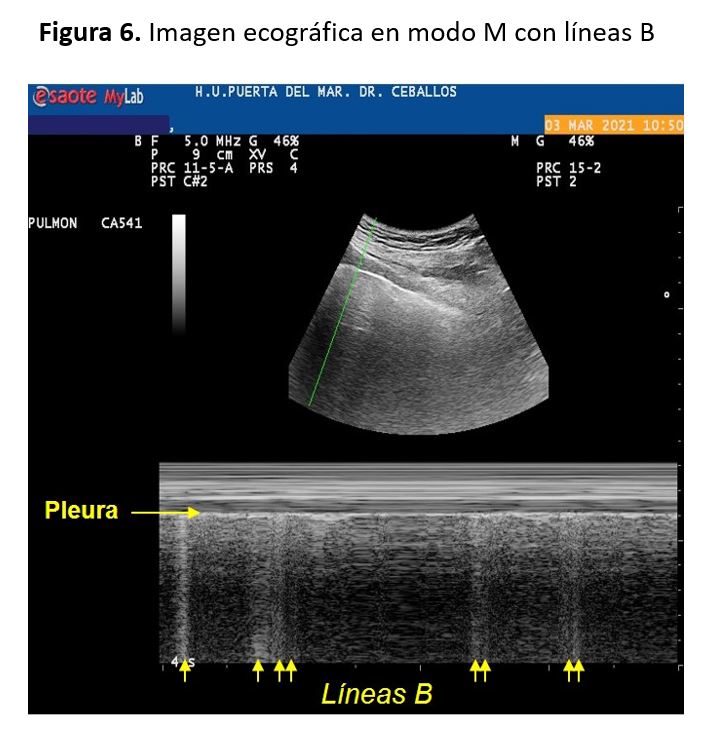
Existen numerosas zonas de evaluación ecográfica, una de ellas consiste en la exploración estructurada de la totalidad del parénquima de forma bilateral, estudiando en cada hemitórax la zona anterior, lateral y posterolateral, delimitadas por la línea mamaria y la línea axilar anterior. Las áreas posteriores pueden ser abordadas con el paciente en decúbito lateral (Figura 5). También podemos emplear el modo M para tener una imagen más detallada de las líneas B (Figura 6).
Ecografía del derrame pleural
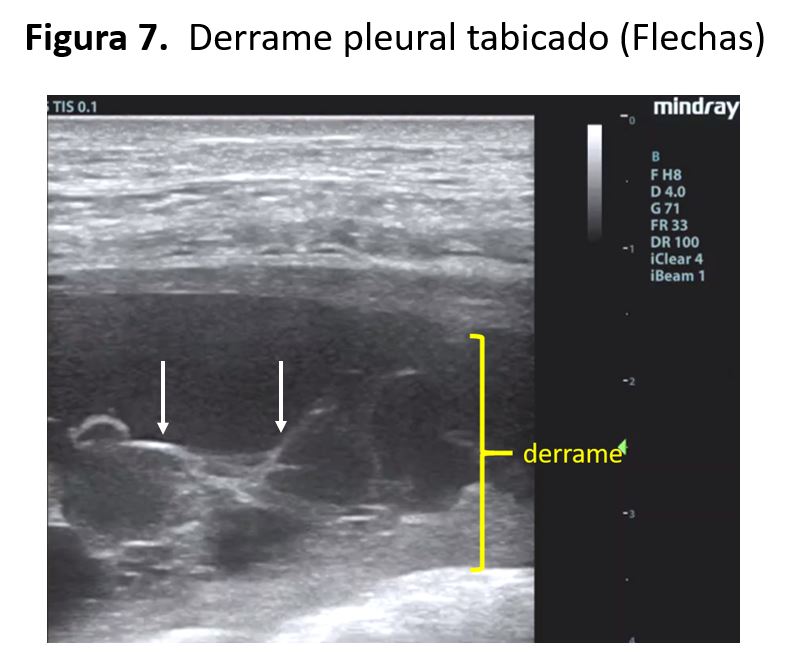
En el derrame pleural ecográficamente se observa una línea ecogénica justo bajo las costillas, seguida de una zona más o menos anecoica (dependiendo de la viscosidad del fluido) y otra línea hiperecogénica, lo que corresponde a la pleura parietal, derrame y pleura visceral, y se conoce como el signo "quad" o signo del límite regular (Figura 7).
El líquido pleural se ubica entre la pleura visceral y la pleura parietal, acumulándose en las porciones más declives (ángulos costo frénicos).
También pueden apreciarse en modo M variaciones del espacio interpleural con el ciclo respiratorio que disminuyen con la inspiración, lo que se conoce como "signo del sinusoide". Cuando el derrame es de importante cuantía se puede apreciar en la base pulmonar atelectasias compresivas (como si el pulmón flotara en el derrame), imagen conocida como "signo de la medusa" (jellyfish sign) o de la lengua (tongue-like sign).
Técnica del estudio del derrame pleural
Emplearemos la sonda convex de baja frecuencia (2,5-5MHz) o en delgados la sonda lineal de alta frecuencia (5-10MHz).
Exploraremos al paciente preferiblemente en sedestación, situando el transductor en transversal, empezando desde la línea axilar anterior hacia la región paravertebral, descendiendo caudalmente. Así conoceremos los límites superior e inferior.
La ecografía es capaz de detectar hasta 5 ml de líquido pleural, y aumenta su sensibilidad cuando hay acumulados más de 30ml, mientras que la radiografía de tórax habitualmente precisa para su detección que se acumulen al menos 75 ml, y cantidades superiores cuando se realiza en decúbito supino (>500 ml).
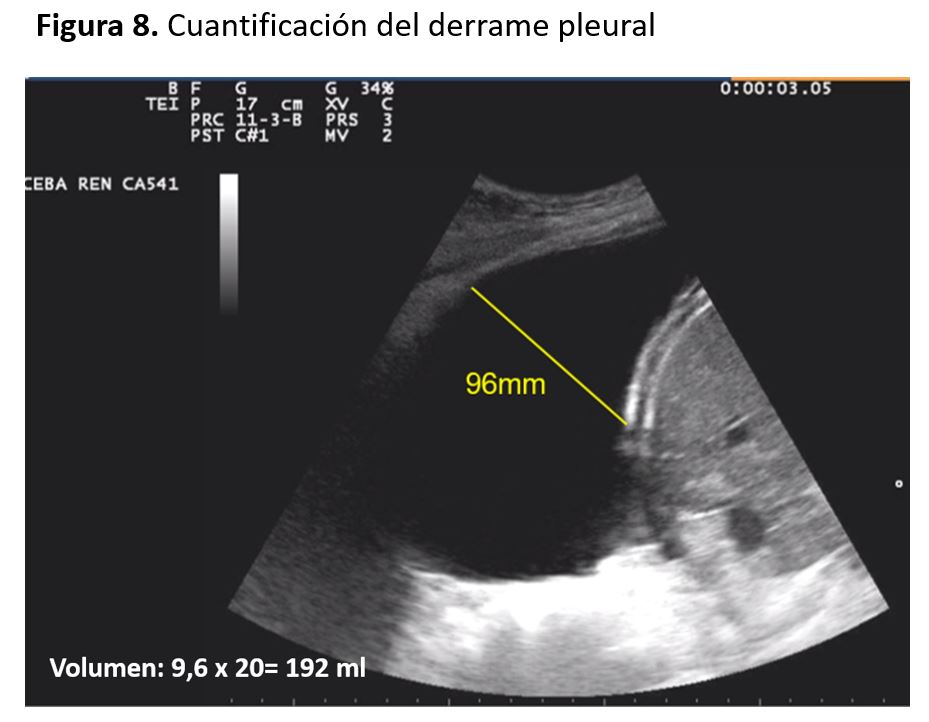
Existen numerosas fórmulas para cuantificar el derrame pleural, siendo una de las más utilizadas la propuesta por Balik et al, donde el volumen estimado (ml) resulta de multiplicar la distancia interpleural máxima (en mm) por 20 [9] (Figura 8).
Ecografía en la condensación pulmonar
La ecografía es una técnica altamente sensible y de gran utilidad para la identificación de focos de condensación, así como para el control evolutivo de los mismos, sobre todo con aquellas neumonías que están en contacto directo con la pleura que, afortunadamente, representan un alto porcentaje.
En los casos de consolidación en el parénquima pulmonar puede apreciarse que el borde más profundo se observa muy difuminado y mal definido en la imagen ecográfica, con áreas habitualmente irregulares de ecogenicidad variable en su interior, alternando zonas con broncograma aéreo, colapso total y un patrón tisular o hepatización, o incluso de absceso [6].
Son varios los criterios diagnósticos que nos pueden confirmar la presencia de una consolidación pulmonar mediante ecografía [10] [11][12] [13]:
- Patrón «tisular»: similar al del tejido de órganos sólidos como el hígado. Único criterio imprescindible.
- Borde pleural superior regular con irregularidad del borde más profundo.
- Ausencia de artefactos (líneas A o B).
- Ausencia del "signo del sinusoide" en modo M, lo que la distingue de un derrame pleural en aquellos casos en los que presenta una ecogenicidad reducida.
- Presencia de broncograma aéreo y alveolograma aéreo: imágenes hiperecogénicas puntiformes o lineales. Representan el aire en el interior de los bronquios o alvéolos rodeados del pulmón consolidado.
- Visualización de arterias y venas pulmonares intraparenquimatosas.
Ecografía del neumotórax
Hoy en día gracias a la colocación eco guiada de los catéteres venosos centrales en la mayoría de los centros hospitalarios, nos encontramos con menos incidencia de neumotórax. Sin embargo, no deja de ser una complicación aguda importante y, por lo tanto, no debe pasar desapercibida dado el riesgo vital que conlleva.
Una manera rápida y precoz de diagnosticarla es mediante ecografía, técnica muy sensible (90-100%) incluso para los neumotórax de pequeño tamaño (ocultos en la radiografía de tórax), en la que podemos distinguir los siguientes signos ecográficos [14]:
1- Ausencia de deslizamiento pulmonar debido a que la pleura visceral pierde el contacto con la pleura parietal.
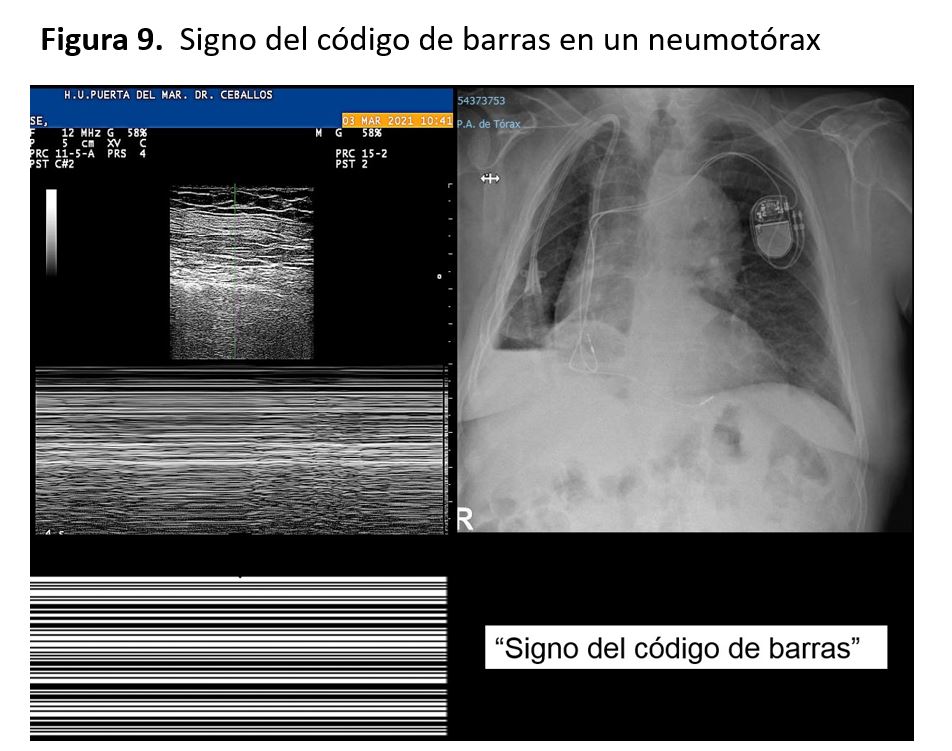
2- En modo M:
Pérdida de la apariencia en "orilla de playa" (Figura 2)d.
Signo de la estratosfera o código de barras (se visualizan líneas horizontales paralelas) (Figura 9).
Signo del punto pulmonar o "lung point": 100% específico. Se aprecia como una sucesión de imágenes normales (arenosas) durante la inspiración y anormales (líneas horizontales) durante la espiración que se corresponden con el punto en el que el pulmón toca la pared torácica con la inspiración, siempre y cuando el neumotórax no sea masivo.
La presencia de líneas B nos permite descartar un neumotórax, dado que implica contacto entre ambas hojas pleurales (Figura 3).
Limitaciones de la ecografía pulmonar
La ecografía pulmonar será menos rentable en aquellos pacientes muy obesos, en los que sería mejor utilizar el transductor convexo ya que alcanza mayor profundidad. También será difícil de realizar en aquellos pacientes que tengan apósitos, drenajes o vendajes torácicos. En el abordaje posterior la presencia de la escápula puede dificultar la visualización de patología a dicho nivel. Por último, la anasarca severa también complica esta exploración.
CONCEPTOS CLAVE
Disponer de un ecógrafo a la cabecera del paciente hace que se pueda diagnosticar de manera certera a una gran proporción de pacientes con disnea en pocos minutos.
Esta técnica de imagen es relativamente fácil de aprender y rápida, ya que requiere entre 5-15 minutos para su realización [15].
Está exenta de complicaciones y de radiaciones, por lo que permite un seguimiento dinámico y continuo.
Tener en cuenta las limitaciones de interpretación en pacientes con enfermedades pulmonares crónicas, dado que presentan alteraciones relevantes de base y algunos cambios pueden pasar desapercibidos.