Osteoporosis en la Enfermedad Renal Crónica. Tratamiento
Introducción
La osteoporosis (OP) y la enfermedad renal crónica (ERC) aumentan con el envejecimiento de la población, condicionando un aumento exponencial de la incidencia de fracturas por fragilidad y sus consecuencias [1] [2] [3] [4]. De hecho, pendientes de la publicación de las últimas controversias KDIGO sobre las alteraciones del metabolismo óseo-mineral (CKD-MBD por su acrónimo inglés), se impone en este sentido el nuevo término “OP asociada a la ERC” [5]. Hemos descrito que la ERC y el complejo CKD-MBD están también asociados a un envejecimiento acelerado [6] y múltiples estudios apoyan la hipótesis de que la ERC produce también un envejecimiento prematuro del esqueleto, aumentando la incidencia de fracturas ya en estadios tempranos (ERC estadio 2) y con un riesgo relativo mayor a edades más jóvenes [7] [8] [9].
Por otra parte, en la primera parte de esta revisión [1] se muestra que, especialmente en estadios tempranos de ERC y sin presentar anormalidades bioquímicas significativas asociadas a CKD-MBD, el riesgo de fractura de estos pacientes podría estar más condicionado por la OP “primaria” (postmenopáusica y senil) que asociada a la propia “osteodistrofia renal” (ODR) [10] [11] . De hecho, en los últimos años, a pesar de las evidentes mejorías en el tratamiento del hiperparatiroidismo y/o la hiperfosfatemia, la incidencia de fracturas por fragilidad no parece haber disminuido [12]. Aunque existen datos que muestran que corregir dichas alteraciones puede disminuir el riesgo de fractura [13] [14] los estudios no son suficientes, por lo que es necesario valorar la presencia de factores de riesgo de OP clásicos que presentan los pacientes con ERC. Por todo ello, consideramos que el nefrólogo debe valorar el riesgo de fractura de forma proactiva, tal y como se recomienda en las guías de práctica clínica para la población general [1] [2].
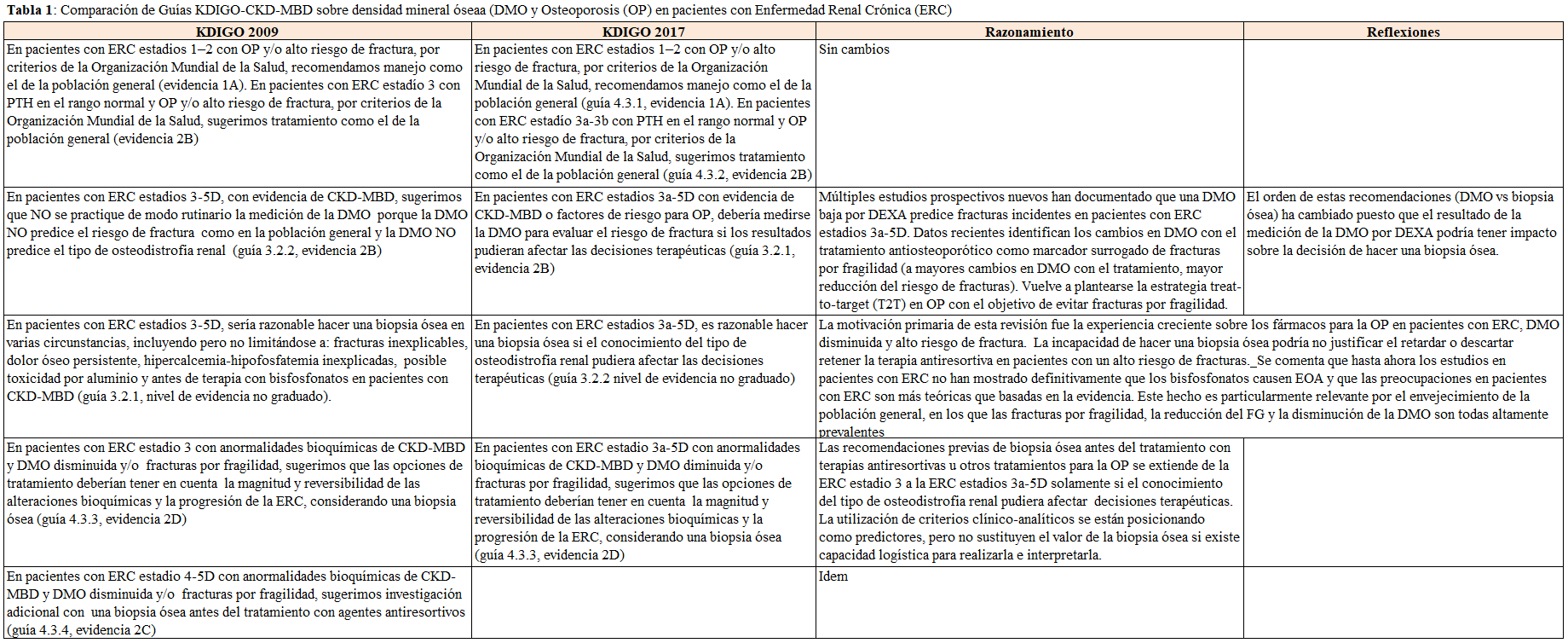
Si bien las guías clínicas abordan este tema [15] [16] (Tabla 1), los nefrólogos no valoran sistemáticamente el diagnóstico y el tratamiento de la OP en pacientes con ERC. Una posible explicación es el condicionamiento terapéutico a la práctica de una biopsia ósea en pacientes con filtrado glomerular (FG) < 30 ml/min/1,73m2 [15] esencialmente indicada para descartar la presencia de una enfermedad ósea adinámica (EOA) u osteomalacia. Sin embargo, las nuevas guías KDIGO 2017 (implementadas por las KDOQI americanas) anteponen la medición de la densidad mineral ósea (DMO) (guía 3.2.1) a la práctica de biopsia ósea (guía 3.2.2) [17] [18] (Tabla 1) y afirman que la incapacidad de biopsiar no debería impedir el uso de terapias antiresortivas, al menos en algunos pacientes [17] [18] con el fin de evitar una actitud nihilista ante un problema importante [1] [2] [4]. En este sentido, distintos grupos de trabajo nacionales y europeos se han afirmado recientemente en esta línea más pragmática a través de distintos consensos y en las propia actualización 2021 de las guías españolas de metabolismo mineral en la ERC [19] [20] [21] [22].
En esta segunda parte, y en espera de estudios prospectivos más amplios específicos en la ERC, revisaremos la evidencia existente sobre los tratamientos destinados a incrementar la DMO y prevenir el riesgo de fracturas, así como el riesgo/beneficio asociado al uso de dichos fármacos en la población con ERC. Asimismo, constatamos la publicación reciente de diversos algoritmos orientativos para el diagnóstico y tratamiento de la osteoporosis tanto en la población general como para pacientes con ERC [19] [20] [23].
Medidas generales no farmacológicas
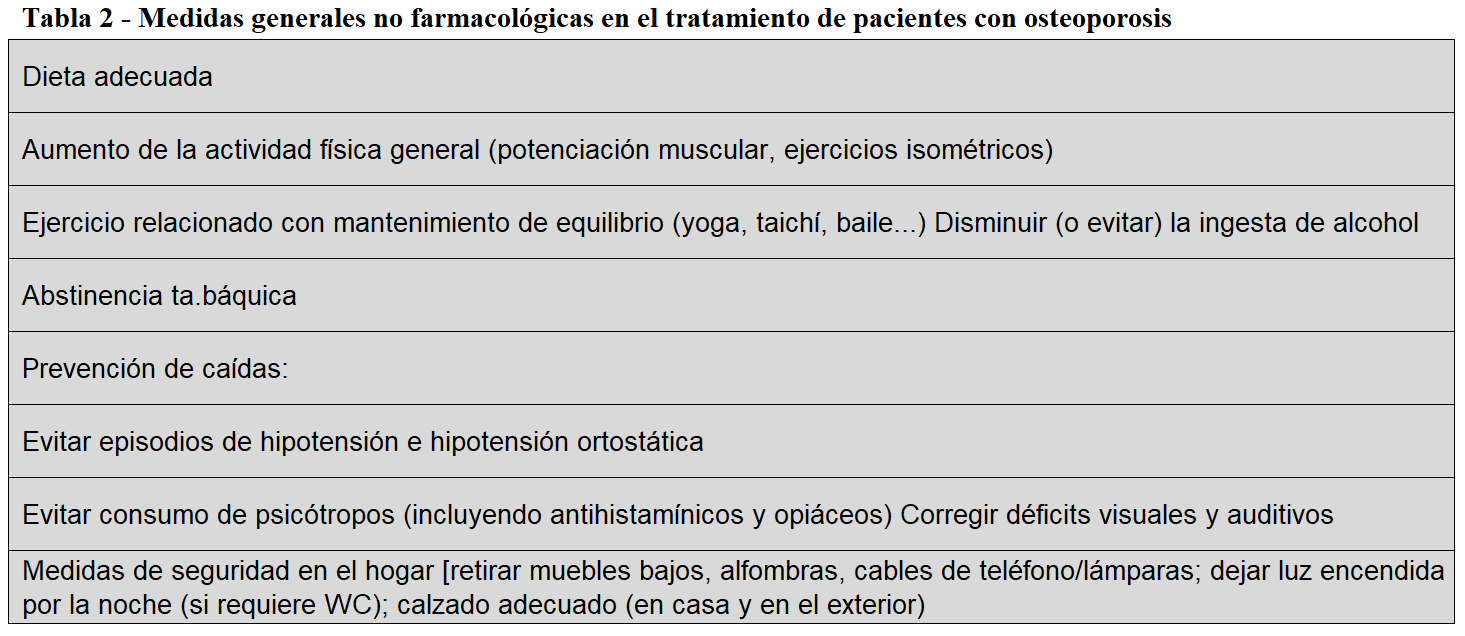
El objetivo final en el tratamiento de la OP es la prevención de las fracturas y sus consecuencias [24]. En 2017, se publicó un consenso español con diferentes especialistas en el que se consideraron objetivos adecuados (“treat to target”) la ausencia de nuevas fracturas, la reducción del riesgo de fractura (FRAX®) y el aumento de la DMO (T>-2,5 para columna y T>-2,5/-2,0 para cuello femoral) [25]. Para ello se consideran importantes (Tabla 2) los cambios en el estilo de vida como hábitos dietéticos saludables, incrementar la actividad física y el ejercicio (yoga, taichí, baile…), disminuir el alcohol y abstinencia tabáquica [26] [27].También es imprescindible tomar medidas para prevenir caídas, fundamentalmente en pacientes de edad avanzada, deterioro cognitivo y funcional, caídas previas, hipotensión ortostática o consumo de psicotropos (incluyendo antihistamínicos y opiáceos) [24] [26] [27] [28]. Osteoporosis y sarcopenia (osteosarcopenia) es una asociación bien documentada en pacientes frágiles [29]. Otras acciones importantes son corregir déficits visuales y auditivos, así como adecuar el entorno físico [26] [29] [30] [31]. Aproximadamente el [30% de los >65 años sufren una caída al año, y el 40% entre aquellos >80 años; de estas caídas un 5% ocasionará una fractura [27]. Todas estas acciones deberían ser también implementadas en pacientes con ERC [6].
Suplementación con calcio y vitamina D
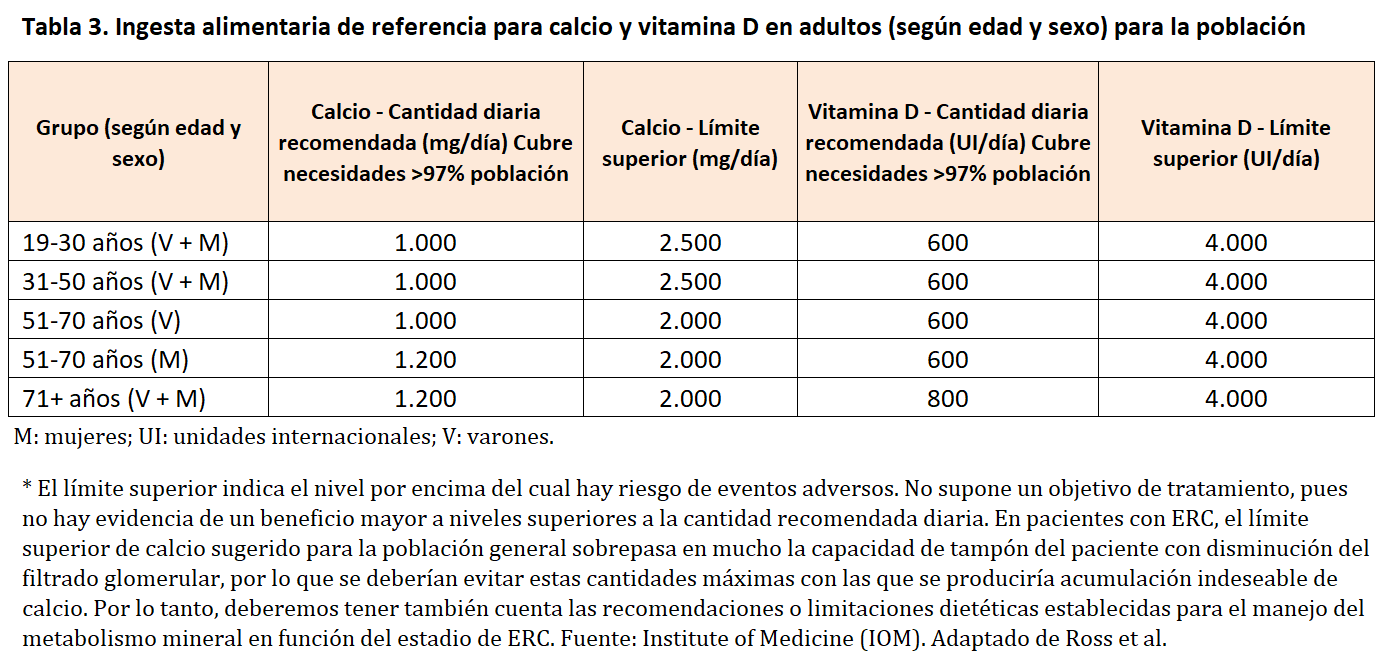
Las guías clínicas destinadas a la población general recomiendan la suplementación de calcio y vitamina D como complemento al tratamiento en pacientes con OP [30]. La baja ingesta de calcio por dieta puede predisponer a largo plazo a desarrollar una OP, aunque los suplementos de calcio con vitamina D se asocian con reducción de fracturas, por si solo es insuficiente para evitar la pérdida de DMO relacionada con la edad o la menopausia [31] [32] [33] [34]. Además, hay datos controvertidos que sugieren que los suplementos aislados de calcio (sin vitamina D) podrían incluso aumentar el riesgo de fractura de cadera [34]. Otras asociaciones negativas descritas de su uso indiscriminado son el incremento del riesgo de nefrolitiasis, arritmias y riesgo cardiovascular, aunque estos resultados son poco concluyentes o contradictorios [1] [6] [26] [31] [33] [35] [36]. El consumo de un aporte excesivo de calcio exógeno en adultos puede ser especialmente perjudicial en pacientes con ERC (o ERC “oculta”) [17] [37] [38] especialmente en presencia de hipercalcemia, hipoparatiroidismo relativo (PTH normal o baja en ERC), EOA, pacientes tratados con warfarina y/o con calcificaciones cardiovasculares [15] [17]. Por ello, un enfoque razonable es alentar preferiblemente como primera medida un consumo apropiado de calcio en la dieta [39] [40] [41], exposición solar diaria prudente y no utilizar rutinariamente la suplementación farmacológica [17] [26] [30] [37] [38] [40], ni los captores cálcicos [13]. La ingesta de calcio recomendada para la población general estaría en torno a los 1000-1200 mg/día [40] (Tabla 3), en función del paciente y de la edad, pero deben tenerse también en cuenta las recomendaciones o limitaciones dietéticas establecidas para el manejo del metabolismo mineral en función del estadio de ERC [12] [17] [37] [38].
La sobrecarga de fosfato (con efectos directos e indirectos sobre la fragilidad ósea) [4] [42] también debería evitarse en pacientes con ERC, sobre todo el fósforo procedente de alimentos procesados, fácilmente absorbible [17]. El uso de captores de fósforo basados en calcio se ha asociado a un aumento de la progresión de calcificaciones vasculares [17] [43] aunque su restricción no ha demostrado definitivamente un aumento de supervivencia [44]. Sin embargo, trabajos recientes prospectivos como COSMOS [45] [46], metanálisis [47] [48] y las nuevas guías KDIGO 2017 [17], enfatizan la necesidad de restringirlos.
La deficiencia de vitamina D es muy frecuente en pacientes con ERC, pero el uso de la vitamina D nativa (i.e. colecalciferol) en ERC tampoco está claramente establecido [17] [49] [50] [51]. Las guías españolas actuales recomiendan la suplementación de vitamina D nativa si los niveles de calcidiol (25-OH vitamina D) son inferiores a 20-30 ng/ml [16] [52] [53]. Las dosis recomendadas para la población general están en torno a las 600-800 UI/día [40] (Tabla 3) y de unas 1.000 UI/día para pacientes con OP, aunque debe individualizarse en funcion de los valores del paciente. La suplementación con vitamina D nativa, incluso en pacientes en diálisis, mejoraría la mineralización ósea aunque con un efecto limitado en la reducción de la PTH [4] [34] [54].
Estos suplementos, en especial el calcifediol (o calcidiol), frecuentemente utilizado en España, se deben administrar a dosis bajas con monitorización frecuente de calcio y fósforo, puesto que no es infrecuente una administración errónea por parte del paciente. Es importante remarcar también que la vitamina D nativa en posología diaria y en pacientes con déficit de vitamina D podría contribuir modestamente a aumentar la fuerza muscular y a disminuir el riesgo de caídas [40] [53] [55] [56] [57]. Sin embargo, se ha publicado recientemente un meta-análisis en el que no se observa menor riesgo de fractura con el uso de calcio, vitamina D o ambos en 51.145 individuos de la población general >50 años no institucionalizados [58]. Los resultados de este estudio no son aplicables a pacientes con OP, otras enfermedades metabólicas o los que toman medicaciones protectoras del hueso como ha sido destacado por la American Society for Bone and Mineral Research.
De este modo, múltiples estudios demuestran que la probabilidad de respuesta inadecuada a otros fármacos para la OP es mayor en pacientes con niveles de calcidiol menores de 20-30 ng/ml [59] [60] y que la corrección del déficit de vitamina D también es necesaria para prevenir casos, no infrecuentes, de osteomalacia [61] (p.ej. en pacientes con niveles bajos de calcio, calcidiol y/o fósforo, frecuentemente con fosfatasa alcalina desproporcionadamente elevada, con dolor óseo importante o múltiples fracturas) [4] [61] [62].
Por último, y junto a la restricción de fósforo, el uso de metabolitos activos de la vitamina D (p.ej. calcitriol, paricalcitol) ha sido uno de los pilares clásicos del tratamiento del hiperparatiroidismo secundario y/o la ODR de alto recambio; no obstante, existe todavía debate sobre su uso apropiado en pacientes con ERC [17] [18] [49] [50]. Los derivados de la vitamina D son los únicos fármacos indicados específicamente para el control del hiperparatiroidismo secundario antes del inicio de diálisis [63] [64] se han asociado a un aumento de supervivencia [65] [66] y se sugiere usarlos de modo juicioso para evitar hipercalcemia, hiperfosfatemia o una excesiva supresión de la PTH [16] [67] [6] [3].
El uso de colecalciferol, ergocalciferol, calcifediol, alfacalcidol y/o calcitriol podría ser efectivo (aunque no plenamente demostrado), junto a bisfosfonatos, en pacientes con exposición prolongada a corticoides [26] [69].
Fármacos antirresortivos para el tratamiento de la OP
Bisfosfonatos
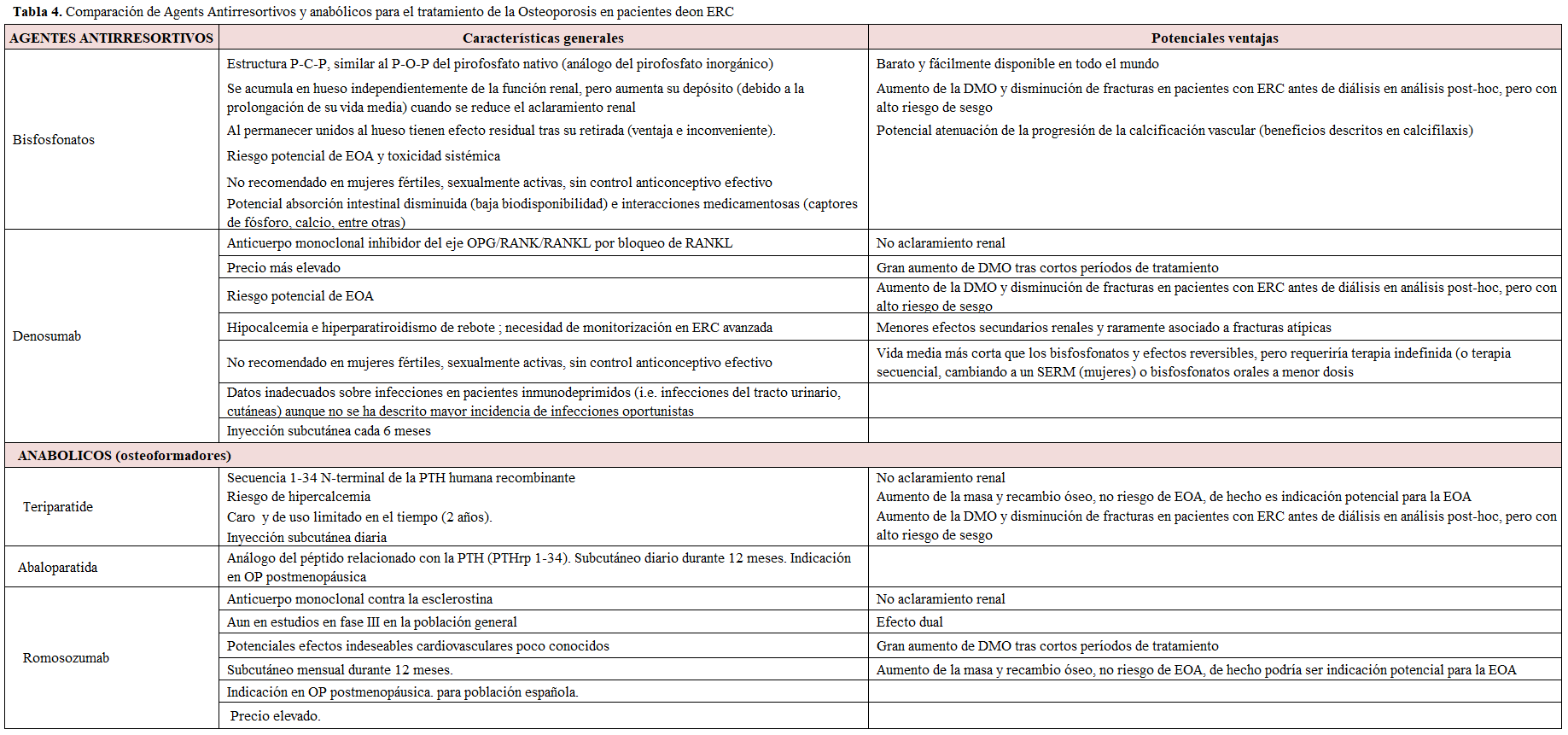
Los bisfosfonatos son análogos estructurales del pirofosfato inorgánico, regulador de remodelación ósea [70] (Tabla 4).Se diferencian entre ellos por el radical 1 y radical 2, proporcionándoles diferente afinidad para la hidroxiapatita y distinta potencia antiresortiva. En relación a su alta afinidad a los cristales de hidroxiapatita, su retención esquelética podría ser de hasta 10 años [70] [71]. La potencia antirresortiva viene determinada, en parte, por la capacidad de inhibir la actividad de los osteoclastos e inducir su apoptosis [66] [72].
Los bisfosfonatos son fármacos de primera elección en el tratamiento actual de todos los tipos de OP, sustentado en los años de experiencia clínica, múltiples indicaciones en diferentes tipos de alteraciones óseas metabólicas y su bajo coste [73] [74] [75] [76]. La dificultad de absorción en las presentaciones orales (alendronato, risedronato) y el riesgo de esofagitis condicionan que su toma se realice en ayunas, con agua, en posición erguida y requieran esperar 30 minutos antes de una nueva ingesta. En las guías KDIGO 2009 (Tabla 1), se sugería que los pacientes con ERC estadios 1 y 2 con OP y/o alto riesgo de fractura, estadio 3 y PTH en el rango normal, siguieran el mismo tratamiento indicado en la población general [15]. De hecho, los pacientes con ERC estadios 1-3 suelen tener pocas anormalidades identificables del metabolismo mineral, compartiendo los mismos factores de riesgo que la población general [77]. Por otra parte, en pacientes con ERC estadio 3 con anormalidades bioquímicas propias de CKD-MBD y disminución de la DMO y/o fracturas por fragilidad, se sugerían otros factores para la elección del tratamiento [15] (Tabla 1). Finalmente, en ERC estadios 4-5D se sugería investigación adicional con una biopsia ósea antes de terapia con agentes antiresortivos [15].
Hoy sabemos que con el deterioro de la función renal, la prevalencia de OP asociada a la ERC aumenta [78] y, especialmente en estadios 4-5D, otros factores casi universales (ODR, acidosis metabólica, hipovitaminosis D, exceso de FGF23, hiperparatiroidismo, resistencia esquelética a la PTH…), complican el diagnóstico de OP basado en DMO. A pesar de que la biopsia ósea sea el único método que permite excluir otras alteraciones en presencia de ERC avanzada, existe un creciente consenso en que basar los tratamientos para OP en la necesidad de una biopsia ósea podría limitar inadmisiblemente el tratamiento en pacientes que presentan un riesgo muy elevado de fractura [19] [20] [21]. Los bisfosfonatos parecen prevenir la pérdida de DMO en la ERC [79] [80] [81] pero no han probado su efectividad en la reducción del riesgo de fracturas en este grupo de paciente por lo que se aconseja un uso individualizado [2] [19] [20] [21] [77] [82]. La firma de un consentimiento informado podría ser necesario cuando se considera su uso fuera de las recomendaciones de ficha técnica [19] [20] [21].
Si bien es cierto que en un reciente trabajo de consenso se plantea el uso de FRAX® + DMO como potencial objetivo terapéutico, se recomienda evaluar el riesgo de fractura a los 3-5 años de bisfosfonato oral o parenteral y plantear la posibilidad de realizar ”vacaciones terapéuticas” o interrupción temporal del tratamiento [26]. Sin embargo, los pacientes que presentan fracturas por fragilidad previas o incidentales durante el tratamiento, DMO en cadera inferior a -2.5 DE, edad superior a 75 años u otras comorbilidades o factores de riesgo que predispongan a fracturas (como por ejemplo fármacos osteopenizantes o caídas de repetición) se recomienda continuar con el fármaco antiosteoporótico (mismo fármaco o cambiar de tratamiento si se considerase respuesta inadecuada) [26] [83] [84]. Disponemos de estudios de seguridad y eficacia a largo plazo con bisfosfonatos, con alendronato (estudio FIT y FLEX a 10 años), risedronato (estudio VERT yVERT-NA a 7 años) o zoledronato (estudio HORIZON a 6 años) [26] [21] [84][85] [86] [87] [88] [89] [90] [91]. Además, los pacientes con una DMO en cadera inferior a -2.5 DE o con fracturas vertebrales prevalentes serían los pacientes con mayor beneficio en completar bisfosfonatos a largo plazo, con una reducción de fracturas vertebrales [84] [85] [92].
El objetivo de la interrupción temporal del tratamiento (o “vacaciones terapéuticas”) tiene el objetivo de aprovechar el efecto residual del fármaco (retención esquelética) y minimizar el riesgo de presentar efectos secundarios asociados al tratamiento a largo plazo, como son la osteonecrosis de mandíbula (ONM) y las fracturas atípicas de fémur (subtrocantéreas-diafisarias). En lo que refiere a la ONM, hay varios factores que predisponen a su desarrollo como son de una predisposición individual, la presencia de diabetes mellitus, el uso de bisfosfonatos por vía endovenosa (i.e. zoledronato), el tratamiento con glucocorticoides y otras comorbilidades como la presencia de una neoplasia o una inmunodeficiencia; así como también problemas buco-dentales como pobre higiene bucal, enfermedad periodontal (o periodontitis), uso de dentadura y la historia de procedimientos dentales, especialmente si éstos son múltiples [70] [83] [93] [94]. El riesgo de ONM se estima entre 1/10.000 y 1/100.000 pacientes-año con bisfosfonatos [26] [27] [93] [95] [96] [97]. En relación a las fracturas atípicas de fémur, estas se asocian al uso de fármacos antirresortivos a largo plazo, aunque también se han descrito en población general sin fármacos antiosteoporóticos. Los factores de riesgo de desarrollar una fractura atípica de fémur son el tratamiento concomitante con glucocorticoides, la raza asiática, un bajo índice de masa corporal y la propia geometría del fémur [84] [98] [99]. Sin embargo, éstas fracturas tienen una predisposición individual genética a su desarrollo [26] [95] [100]. Es importante señalar que es necesario tratar 40 mujeres con ácido alendrónico durante 10 años para evitar 25 fracturas de cadera; mientras que por el contrario, es necesario tratar 885 mujeres con alendronato durante 10 años para causar 1 fractura atípica de fémur. Por ello, el beneficio del tratamiento con bisfosfonatos es claramente superior al riesgo de producir una fractura atípica de fémur [26] [27].
Finalmente, la inhibición de la actividad osteoclástica inducida por bisfosfonatos ha generado la duda respecto a la posibilidad de generar un “hueso adinámico” por excesiva supresión del remodelado óseo y, por tanto, menor capacidad para la reparación de microfracturas y mayor fragilidad esquelética [70] [101] [102]. Es conocida la afinidad del bisfosfonato al hueso y su retención esquelética [103]. De todos modos, en perros tratados con altas dosis de bisfosfonatos se ha observado un incremento de microfracturas [104] y un estudio reciente mostró menos porosidad pero más microfracturas en los huesos fracturados de pacientes tratados con bisfosfonatos comparados con pacientes con fractura no tratados o controles sanos [105]. Sin embargo, biopsias de cresta ilíaca realizadas tras 5-10 años de tratamiento no parecen mostrar sobresupresión del remodelado óseo [106] [107] [108] o, en otros trabajos, no se ha observado aumento de microfracturas [109] [110]. En este sentido, datos de un estudio con alendronato en mujeres postmenopáusicas sugieren que incluso una prolongada reducción del recambio óseo es improbable que se asocie a efectos adversos sobre las propiedades del hueso [111]. Asimismo, es motivo actual de debate si la disminución de recambio óseo per se o la enfermedad que lo causa (i.e. diabetes, inflamación crónica, estrés oxidativo, malnutrición) serían las responsables del incremento del riesgo de fractura apreciado en estos pacientes [19] [112] dado que la reducción del recambio óseo secundario a paratiroidectomía o terapias farmacológicas (calcimiméticos, antirresortivos) no se asocia a mortalidad prematura ni calcificación vascular acelerada en los pacientes con ERC [112]. Independientemente del riesgo moderado de progresión de la ERC valorada por criterios discutibles (cambio de estadio) en pacientes con ERC G3b-5, el tratamiento con bisfosfonatos se asoció a mejoría de la supervivencia al menos en una de las cohortes analizadas [113]. Por todo ello, la duración óptima de la terapia con bisfosfonatos debiera ser individualizada en función de los factores de riesgo del paciente y, aunque el riesgo parece bajo incluso en tratamientos hasta 10 años [83] [108] queda pendiente valorar el riesgo/beneficio del uso prolongado en pacientes con bajo riesgo de fracturas o pacientes con ERC avanzada [6] [114].
En cuanto a los bisfosfonatos en la ERC, es bien conocida la contraindicación de los bisfosfonatos endovenosos con aclaramientos de creatinina por debajo de 30 ml/min y que éstos pueden producir diversos tipos de daño renal [115] [116]. Sin embargo, en un análisis post-hoc de los ensayos clínicos con alendronato y risedronato oral que incluyeron pacientes con disminución del FG (ERC estadios 3-4), durante un máximo de 3 años, no hubo diferencias en la aparición de efectos renales adversos [79] [80]. En una cohorte binacional se ha descrito un discreto incremento de riesgo de progresión de la ERC con el uso de bisfosfonatos [117]. Los bifosfonatos quedan retenidos en el hueso por su afinidad con la hidroxiapatita [103], estos podrían tener mayor acúmulo en el hueso del paciente renal [118] [119] (Tabla 4). En las guías KDIGO 2009 sugerían la práctica previa de una biopsia ósea antes de iniciar bifosfonatos en pacientes con ERC estadios 4-5 (Tabla 1) [15] basándose en un estudio transversal con 13 pacientes con ERC estadios 2-4 a los que se les practicó una biopsia ósea tras un período variable de tratamiento con bisfosfonatos (4->60 meses), siendo todos ellos diagnosticados de enfermedad ósea dinámica [120].
En el contexto del trasplante renal, Coco et al, mostraron que 6/6 pacientes tratados con pamidronato e.v. (con una frecuencia de administración muy superior a la habitual) presentaron EOA vs 3/8 en los controles, si bien las alteraciones óseas pretrasplante se desconocían [120]. Adicionalmente, sólo 14/72 pacientes fueron biopsiados, por lo que es difícil extrapolar estos datos. Actualmente la prevalencia de EOA está en aumento [67] [118] [121] e incluso podría preceder a la enfermedad de alto recambio durante la evolución de la ERC [122] [123].
Por ello, en pacientes con ERC y OP, previo a la indicación de bisfosfonatos debería valorarse la presencia de factores de riesgo de enfermedad ósea dinámica como son la diabetes, la sobrecarga de calcio, la malnutrición, la inflamación, el hipoparatiroidismo relativo (niveles de PTH bajos o relativamente bajos) o el propio envejecimiento si está asociado a estos factores [67] [118] [124]. De hecho, de acuerdo con las fichas técnicas y dada su exclusión de los estudios pivotales, el tratamiento con bisfosfonatos en pacientes con ERC con aclaramientos de creatinina < 30-35 ml/min estaría contraindicado y, tal como se ha comentado, en caso de usos fuera de ficha técnica se debería solicitar un consentimiento informado formal del paciente [19] [20] [22] [125]
Sin embargo, tras la publicación de las guías KDIGO 2009 [15] se ha demostrado que la DMO sí predice el riesgo de fractura en pacientes con ERC [126] [127] [128] [129]. Otros análisis post-hoc de grandes ensayos aleatorizados (alendronato, risedronato) centrados en el tratamiento de la OP postmenopáusica han descrito que estos fármacos tienen una eficacia comparable en pacientes (especialmente mujeres) con ERC (la mayoría en estadios 3-4), mejorando la DMO y reduciendo el riesgo de fracturas [79] [80]. Por ello, al menos en ausencia de anormalidades significativas en el metabolismo óseo mineral, el uso de bisfosfonatos y otros fármacos aprobados para el tratamiento de OP podrían ser apropiados en pacientes con niveles de creatinina “normales” y un FG disminuido [2] [17] [18] [79] [80]. De este modo, en la actualización de las KDIGO 2017 [17] (Tabla 1), la necesidad de una biopsia ósea previa no es obligada en pacientes con ERC avanzada. De hecho, se considera que no se ha demostrado de modo fehaciente que los bisfosfonatos causen EOA y que la experiencia acumulada con fármacos antiresortivos permitirían considerar su uso aún sin biopsia [17], aunque sin descartarla si existe la posibilidad logística [130] . Como se ha comentado con anterioridad, es motivo actual de debate si es la disminución de recambio óseo per se o la enfermedad que lo causa el responsable del incremento del riesgo de fractura apreciado [19] [112].
Así, la “dificultad” de practicar o interpretar histomorfométricamente una biopsia no justificaría el nihilismo terapéutico en pacientes con un alto riesgo de fractura [17] [130]. Más allá de las guías, debemos reconocer que otros análisis resaltan que no se han mostrado efectos beneficiosos consistentes más allá de la DMO y que no existe evidencia absoluta sobre la disminución del riesgo de fractura o la calcificación vascular [82]. Sin embargo, en paralelo también se está posicionando la DMO “alcanzada” con el tratamiento antiosteoporótico, como un marcador subrogado de fracturas [131]. En relación a la importancia de la relación hueso-vaso [132] [133] [134], se ha postulado con algunos fármacos efectos incluso potencialmente beneficiosos [135]. Así, a nivel experimental y clínico (en pequeños estudios en pacientes en diálisis) se ha descrito que algunos bisfosfonatos podrían disminuir la progresión de las calcificaciones vasculares o ser efectivos en pacientes con calcifilaxis [136] [137]. Es por ello que hoy se considera que para cualquier fármaco orientado a la disminución de la progresión de la calcificación vascular en pacientes con ERC, se debería incluir valoración de su potencial efecto sobre el hueso, y viceversa [138] . Asimismo, las distintas afinidades por el hueso o características farmacocinéticas/farmacodinámicas de distintos bisfosfonatos (i.e. risedronato) podrían favorecer su uso en pacientes con ERC [139] [140] independientemente de la posibilidad de reducción de dosis o intervalos de dosificación.
Denosumab
Denosumab (DMab) es un anticuerpo monoclonal que actúa bloqueando el ligando del receptor activador del factor nuclear kappa-B (RANKL) y como consecuencia inhibe la osteoclastogénesis [141] [142] (Tabla 4). DMab ha demostrado reducir la incidencia de fracturas vertebrales, no vertebrales y de cadera en la población general [143] [144] [145]. DMab no depende de la función renal para su metabolismo o excreción (el aclaramiento se produce a través del sistema retículo endotelial) y no parece alterar la función renal, por lo que no se necesita ajustar dosis en pacientes con ERC ni tiene restricciones de uso en pacientes con disminución del FG [26] [145]. Al tratarse de un anticuerpo monoclonal, es un fármaco reversible (la molécula se inactiva) y en caso de no administrar un bisfosfonato se produce una marcada pérdida de masa ósea que puede ir acompañada de fracturas vertebrales múltiples (especialmente en individuos con DMab de larga duración, sin bisfosfonatos previo y con fracturas vertebrales previas [146] [26], por lo que es importante conocer su naturaleza y mecanismo de acción.
En análisis post-hoc de mujeres osteoporóticas con ERC estadio 3 (n=2.817) y 4 (n=73) se ha descrito que, tras 36 meses de seguimiento, DMab también incrementa la DMO y reduce el riesgo de fractura vs placebo, independientemente de la función renal y sin efecto sobre la creatinina o la incidencia de efectos adversos [147] (Tabla 4). No obstante, el DMab puede inducir hipocalcemia, especialmente en pacientes con ERC y pacientes en hemodiálisis con alto recambio óseo subyacente [148] [149] [150] [151]. Este efecto potencial es importante y ocasionalmente grave [152] [153] especialmente en el primer mes del tratamiento, debiéndose prestar especial atención en aquellos pacientes de riesgo (mayor a mayor grado de ERC) que estén recibiendo concomitantemente cinacalcet [151] (posiblemente también con etelcalcetida). De considerarse indicado DMAb por la presencia de un elevado riesgo de fractura, deberá informarse al paciente de la sintomatología de hipocalcemia, monitorizar el calcio sérico (idealmente total e iónico) de modo más frecuente y realizarse una reposición más intensa, temporal, de calcio y vitamina D (nativa y/o calcitriol) y/o aumentar transitoriamente el calcio en el baño de diálisis en un intento de “alimentar el hueso hambriento” [147] [148] [154]. La progresión de calcificación aórtica y eventos cardiovasculares, con excepciones puntuales, no ha mostrado diferencias entre DMab y placebo [155] [156]. Como se ha comentado, en pacientes en hemodiálisis, el DMab se propone como un tratamiento relativamente seguro desde el punto de vista de la hipocalcemia [al menos con el habitual baño de 3 mEq/L (1.5 mmol/L) [151] ya que cada sesión procuraría un cierto balance positivo de calcio. Aun así, pacientes y prescriptores deberían estar alerta a la posibilidad de hipocalcemia [154]. Además, a pesar de la administración concomitante de vitamina D, DMab puede producir un aumento (reversible) de PTH intacta que puede llegar a valores superiores a 1000 pg/ml [151].
Varios estudios han mostrado efectos beneficiosos de DMab en pacientes en diálisis. En un estudio piloto prospectivo en 12 pacientes, todos ellos con PTH>1000 pg/mL, DMO con una escala T-score inferior a -1.0 DE y dolor óseo,no candidatos a cirugía, Chen et al [157] describieron los efectos de DMab, calcitriol, captores de fósforo y un baño de calcio ajustado según los datos bioquímicos. La DMO aumentó en cuello femoral y columna lumbar tras 6 meses y se redujo el dolor. En el primer mes, la mayoría de los pacientes experimentaron un aumento de la PTH intacta que rápidamente descendió al final del estudio tras aumentar la dosis de calcitriol (1702±182 a 519±127 pg/mL) [157]. En otro estudio más prolongado, retrospectivo, con 12 pacientes osteoporóticos en hemodiálisis que recibieron DMab, se observó también una mejoría de parámetros de metabolismo óseo y de la masa ósea tras 24 meses de seguimiento, aunque esta sólo fue medida por ultrasonidos de falanges.
Es importante señalar de nuevo la reversibilidad del fármaco ya que tras la interrupción del mismo se produce una marcada y rápida pérdida de masa ósea, que en algunos pacientes puede acompañarse de fracturas vertebrales múltiples incidentales [146]. Por ello, en caso de suspender el tratamiento con DMab es importante iniciar un bisfosfonato para realizar un sellado de masa ósea y minimizar el efecto rebote [158] [26] [30]. Los pacientes con fracturas vertebrales previas (especialmente si más de 4), aquellos que no habían recibido bisfosfonatos previamente, con muy baja masa ósea inicial y con duración del DMab superior a 2-3 años son los de mayor riesgo de presentar fracturas vertebrales múltiples, entre otros factores menos conocidos como la gran ganancia de masa ósea en cadera durante el tratamiento y, por supuesto, la rápida pérdida al suspenderlo [158]. Por ello, debería valorarse de forma individual la necesidad de la retirada del fármaco y asegurar el cambio a bisfosfonato de acuerdo con las recomendaciones de las guías de práctica clínica actuales [159] [158] . Además, es necesario recordar que los bisfosfonatos estarían potencialmente contraindicados por ficha técnica en pacientes con aclaramientos de creatinina inferiores a 30-35 ml/min, dificultando la retirada de DMab en pacientes con ERC.
En resumen, a la luz del conocimiento actual, parece que agentes antiresortivos como bisfosfonatos o DMab podrían usarse al menos en pacientes con fracturas por fragilidad y/o elevado riesgo de fractura [2] [160] en distintos estadios de ERC (especialmente ERC 1-3) de un modo similar al de la población general y sin necesidad de practicar una biopsia ósea si tras la evaluación individualizada del paciente se considera poco probable la presencia de una EOA. Los bisfosfonatos, podrían estar indicados en dichos pacientes especialmente si se observan índices de alto recambio [77] (PTH y fosfatasas alcalinas significativamente elevadas), probablemente espaciando las dosis y/o limitando la duración del tratamiento [77] [161]. DMab podría estar especialmente indicado en pacientes con muy alto riesgo de fractura y extenderse a estadios de ERC más avanzados (i.e. ERC estadio 4 o incluso 5), con especial control de la calcemia. Ensayos clínicos (i.e. con DMab o alendronato en ERC avanzada y diálisis [157] [162] [163] podrían proporcionar información relevante en los próximos años; hasta entonces una opción válida es adoptar algoritmos diagnóstico-terapéuticos basados en el riesgo de fractura y no quedar a la espera de una evidencia absoluta [4] [19] [26] [158] [164].
Fármacos anabólicos (osteoformadores) para el tratamiento de la OP
Teriparatida
Teriparatida (Tabla 4) (PTH 1-34 recombinante humana) está aprobada como terapia osteoformadora (anabólica) para la OP postmenopáusica, OP corticoidea, OP del varón, con elevado riesgo de fractura y, de acuerdo con guías, pacientes con muy alto riesgo de fractura: dos o más fracturas vertebrales; una fractura vertebral o de fémur con DMO < -3.0 DE o muy baja DMO < -3.5 DE) [26] [31] [165]. Actúa incrementando la formación ósea, por la exposición de forma intermitente a la PTH, particularmente en el hueso trabecular, con un menor incremento de la resorción ósea, condicionando un balance positivo de hueso. Tras completar los 24 meses de tratamiento, en caso de no iniciar otro fármaco antiosteoporótico (bisfosfonato o DMab), se produce una pérdida más lenta y atenuada de masa ósea [25] [166]. Sin embargo, aparte de sus contraindicaciones (alergia o intolerancia, hipercalcemia no filiada, radioterapia, neoplasia o metástasis o factores de riesgo de sarcoma como la enfermedad de Paget o edad infantil), también presenta limitaciones como el elevado coste económico y la limitación temporal vigente de que no puede administrarse por periodos superiores a 24 meses (Tabla 4). Esta limitación temporal, con condiciones, es posible que sea relegada en Europa tal y como hizo ya la Food and Drug Administration (FDA) americana retirando la “black box” por la falta de evidencia en humanos sobre el riesgo de osteosarcoma [167] [168].
Comparado con placebo, teriparatida mostró un incremento significativo de la DMO en columna lumbar y cuello femoral y no hubo evidencia de que este incremento de la DMO se modificara por la enfermedad renal [169]. Aunque por ficha técnica su uso es restringido en ERC moderada y contraindicado en ERC severa, un análisis post-hoc reciente mujeres japonesas con OP, ERC estadios 4-5 y alto riesgo de fractura (82% tenían una fractura previa), observándose que teriparatida subcutáneo 20 µg/día durante 24 meses [170].También ha sido descrito que el uso de 56,5 µg de teriparatida, administrado una vez a la semana, aumentó la DMO lumbar en pacientes japoneses en hemodiálisis con hipoparatiroidismo y DMO baja, aunque 10/22 pacientes tuvieron que abandonar el tratamiento por efectos secundarios [171]. Es importante reseñar la descripción de un incremento del recambio óseo en pacientes con enfermedad ósea adinámica confirmada por biopsia ósea [67] [172] [173] . Recientemente ha sido descrito que el uso de 56,5 µg de teriparatide, administrado una vez a la semana, aumentó la DMO lumbar en pacientes japoneses en hemodiálisis con hipoparatiroidismo y DMO baja, aunque 10/22 pacientes tuvieron que abandonar el tratamiento por efectos secundarios [171]. Finalmente, es importante incidir en que teriparatida (también abaloparatida) está especialmente contraindicado, entre otros, en pacientes con neoplasias o metástasis, con antecedentes de radioterapia previa o con elevaciones inexplicadas de fosfatasa alcalina (i.e. Paget).
Independientemente de teriparatida, no podemos olvidar que, en pacientes en diálisis con PTH disminuida (< 2 veces el límite alto de la normalidad y, especialmente, si tienen antecedentes de fractura), existe la posibilidad de disminuir el calcio en el líquido de diálisis para aumentar la PTH endógena y mejorar el remodelado óseo [4] [67]. Por último, destacar que un ensayo clínico en marcha en pacientes con OP en diálisis asigna al brazo de bajo recambio óseo una combinación teriparatide-cinacalcet (NCT02440581), quizá para estimular la producción endógena de PTH por la hipocalcemia inducida por cinacalcet.
Abaloparatida
Es un fármaco osteoformador indicado en mujeres postmenopáusicas con alto riesgo de fracturas. Se trata de un análogo sintético del péptido relacionado con la PTH (PTHrp) 1-34 de reciente comercialización en España. Su pauta es de 80 µg diarios, por vía subcutánea, durante 18 meses y produce un aumento de la osteoformación y una menor activación de la resorción ósea. El estudio ACTIVE ha mostrado mejoría importante en la DMO en columna y cadera, junto con una reducción de fracturas vertebrales, mayores osteoporóticas y fracturas no vertebrales [174] . Por ficha técnica, se indica la realización de un electrocardiograma previo al inicio del tratamiento con abaloparatida por la mayor prevalencia de taquicardia tras la administración comparada con placebo (abaloparatida 1,6 % vs. 0,4 % placebo).
De acuerdo con la ficha técnica, abaloparatida no se debe utilizar en pacientes con ERC grave. De hecho, no se han realizado estudios en pacientes en hemodiálisis. En pacientes con ERC leve a moderada no es necesario ajustar la dosis. En un subanálisis del estudio ACTIVE (estudio pivotal fase III) en el que se analiza la evolución de la DMO en función del aclaramiento de creatinina (>90 mL/min, entre 60 y 90, o <60 mL/min), no se observaron diferencias en eficacia ni en seguridad [175]. Señalar que en este estudio se excluyeron aquellas pacientes con creatinina >2.0 mg/dL o creatinina entre 1.5-2.0 mg/dL y aclaramiento de creatinina<37 mL/min [175]
Romosozumab
Romosozumab (RMab) (Tabla 4) es un anticuerpo monoclonal humanizado contra la esclerostina, inhibidor de la vía Wnt responsable de la formación de hueso. La esclerostina producida por los osteocitos se une a las proteínas LRP 4-5-6, receptores de los ligandos de la vía del Wnt. RMab estimula así la formación e inhibe la resorción ósea, efecto dual, a diferencia de otros fármacos osteoformadores que incrementan la resorción ósea [176] [177]. Estudios clínicos han mostrado mejoría importante en la DMO en columna y cadera [178] [179] [180]. En el estudio ARCH con mujeres postmenopáusicas con muy alto riesgo de fractura se mostró que el tratamiento secuencial con RMab mensual durante 12 meses seguido de alendronato durante 12 meses se asoció con mayor incremento de DMO y menor incidencia de fracturas que las pacientes tratadas solo con alendronato durante 24 meses [180]. Sin embargo, en este estudio se adjudicaron un mayor número de algunos eventos cardiovasculares al grupo de RMAb durante el primer año de tratamiento (2,5% vs 1,9%, respectivamente), aunque no hubo diferencias cuando RMab se comparó con placebo [178] [179] [180]. Por este motivo su administración está contraindicada en pacientes con antecedentes de infarto de miocardio o accidente cerebrovascular (ficha técnica del producto https://cima.aemps.es/cima/pdfs/es/ft/1191411/FT_1191411.pdf). El papel de este fármaco en pacientes con ERC aún es insuficiente para aconsejar su uso [181], aunque existen experiencias preliminares de su uso incluso en pacientes en hemodiálisis con muy alto riesgo de fractura sin aparente incremento de eventos cardiovasculares [181]. No está aclarada aun la posibilidad de que pueda aumentar la progresión de calcificaciones vasculares [182] [183]. Aunque RMab no requiere ajuste de dosis en pacientes con ERC, se sugiere que en las pacientes con insuficiencia renal grave o que se someten a diálisis debe monitorizarse la concentración sérica de calcio (ficha técnica del producto https://cima.aemps.es/cima/pdfs/es/ft/1191411/FT_1191411.pdf) con prudencias similares a las mencionadas previamente con DMab.
Otros tratamientos
Estrógenos y raloxifeno
El hipoestrogenismo es una causa bien conocida de OP y tanto la terapia estrogénica adecuada como el uso de los moduladores selectivos de los receptores de estrógenos (“SERMs” por su acrónimo inglés) han mostrado mejorar la OP postmenopáusica [31]. La menopausia precoz (o hipogonadismo prematuro) es más frecuente en mujeres con ERC [184] por lo que estas pacientes representan una población especial de alto riesgo.
Raloxifeno es un SERM con menor riesgo carcinogénico comparado con la terapia estrogénica clásica (incluso descrito como protector de cáncer de mama) y es una alternativa en la OP postmenopáusica con riesgo moderado de fracturas [185] [186] [187]. Ha demostrado mejorar la DMO y disminuir el riesgo de fracturas vertebrales pero no las de cadera [185] [188]. En un análisis post-hoc en mujeres con aclaramiento de creatinina >20 ml/min, se observó el mismo efecto sobre fracturas vertebrales. Otros estudios con pocos pacientes han descrito que raloxifeno incrementa la DMO y reduce la pérdida de masa ósea en columna, cadera y radio y reduce el riesgo de fractura vertebral en pacientes con ERC [187] [189] (Tabla 4).
Es importante considerar que raloxifeno podría jugar un papel interesante en terapias secuenciales de la mujer con OP [34] [35]. Sus efectos secundarios más frecuentes son sofocos y calambres y la trombosis venosa es su efecto adverso más importante; por ello no se debería utilizar en pacientes con sintomatología climatérica o riesgo de tromboembolismo. No se dispone de experiencia con bazedoxifeno en pacientes con ERC.
Cinacalcet y paratiroidectomía
Además del efecto beneficioso de cinacalcet sobre la ODR [190] un análisis secundario preespecificado del estudio EVOLVE evaluó la aparición de fracturas clínicas en pacientes en diálisis con hiperparatiroidismo secundario [13]. Tras varios ajustes estadísticos, el riesgo relativo de fractura fue discretamente menor con cinacalcet [0,83 (IC 95%, 0,72-0,98)] y, usando otro análisis también pre-especificado (“lag-censoring analysis”), el riesgo relativo de fractura con cinacalcet fue de 0,72 (0,58-0,90) [13]. Cinacalcet no es efectivo en el tratamiento de la disminución de la DMO en hiperparatiroidismo primario.
Si cinacalcet representaría la posibilidad teórica de “paratiroidectomía química”, se ha descrito que la paratiroidectomía quirúrgica sí disminuye el recambio óseo, mejora la DMO y reduce el riesgo de fractura en pacientes en diálisis [4] [191] [192], pero en estos estudios existen numerosos sesgos por indicación y la intervención no está exenta de riesgos [193].
Calcilíticos
No existen todavía en el mercado agentes inhibidores del receptor-sensor de calcio (a diferencia de agonistas como cinacalcet) [194]. Estos fármacos podrían suponer en el futuro un modo indirecto de aumentar la producción endógena de PTH en pacientes con EOA.
Otros
La hiponatremia y la acidosis metabólica se asocian a OP, por lo que sería recomendable evitarlas. La hiponatremia se ha asociado principalmente a fracturas de cadera, de forma indirecta por favorecer alteraciones neurológicas que pueden favorecer caídas y por un mecanismo directo al movilizar de modo compensador las reservas de sodio del hueso en respuesta a la hiponatremia, estimulándose la osteoclastogénesis [195] . Es de recordar que, entre otros efectos, la acidosis metabólica crónica promueve la activación de los osteoclastos, promoviendo así la reabsorción ósea [196]. Por otra parte, distintos estudios experimentales y datos clínicos preliminares han mostrado efectos controvertidos y variables en el hueso tras inhibición del sistema renina angiotensina o con el uso de otros fármacos de interés nefrológico como betabloqueantes, diuréticos, estatinas, antidiabéticos orales, inmunosupresores u omeprazol [197] [198].
Conclusión
Si bien el efecto de diferentes fármacos antiosteoporóticos en la población general no se puede equiparar en términos de eficacia a los pacientes con ERC, la evidencia actual y las nuevas recomendaciones de práctica clínica abogan a una mayor proactividad en el diagnóstico y tratamiento de la OP en estos pacientes. Mientras que en ERC estadios 1-3, sin alteraciones bioquímicas evidentes (que serían siempre el primer objetivo terapéutico en cualquier estadio), se recomienda aplicar las recomendaciones de las guías de práctica clínica para la población general, en estadios más avanzados podrían utilizarse estos fármacos de forma individualizada y consensuada con los pacientes, siendo especialmente importante recordar que el principal factor de riesgo de fractura es el antecedente de una fractura por fragilidad previa [20] [23] [26] [11] [10].
A todos los pacientes se les recomienda un aporte adecuado de calcio por la dieta y la corrección, según los niveles de calcidiol, con vitamina D (i.e. colecalciferol, calcifediol). Los agentes antiresortivos (bisfosfonatos o DMab) podrían usarse de modo seguro y efectivo sin la exigencia de tener que hacer una biopsia ósea previa. Los antiresortivos también podrían usarse en estadios más avanzados en pacientes seleccionados (Tabla 5), siendo de especial relevancia en aquellos individuos con riesgo elevado de fracturas y/o en pacientes con fracturas clínicas o morfométricas previas (que indican fragilidad ósea). Entre los agentes antiresortivos, al no eliminarse por vía renal, DMab sería una alternativa a considerar en presencia de ERC avanzada y su utilización obliga (al igual que con RMab) a un control adecuado de la calcemia y replección con vitamina D (“alimentar el hueso hambriento”, especialmente al inicio del tratamiento), siguiendo directrices recientemente publicadas [154]
En pacientes con muy elevado riesgo de fractura (≥ 2 fracturas vertebrales, una fractura vertebral o de cadera más una DMO T < -3,0 DE ó DMO T < -3,5 DE), podría estar especialmente indicado el uso de un fármaco osteoformador como la teriparatida o la abaloparatida (Tabla 5) siempre con valoración adecuada del riesgo/beneficio, especialmente en pacientes paratiroidectomizados o si se sospecha enfermedad ósea adinámica (para lo que resulta útil analizar no solo la PTH sino los biomarcadores óseos como la fosfatasa alcalina) [4] [19] [22] [199] [200] [201]
A pesar de la actitud proactiva sugerida actualmente en el diagnóstico y tratamiento de la OP en pacientes con ERC, debemos reconocer la necesidad indudable de disponer de ensayos clínicos con inclusión de pacientes con ERC (con y sin CKD-MBD) y/o registros con el fin de actualizar el manejo de estos tratamientos en esta población tan específica y frecuente, dado que la mayoría de estudios realizados hasta ahora no han sido consistentes, tienen sesgos importantes y un bajo grado de evidencia por su carácter post-hoc [82] [119] [160] [202][203].